Det siges ofte, at ca. 80 % af alle hjertestop skyldes akut eller kronisk koronararteriesygdom, hvor sidstnævnte er den mest almindelige. Tallet 80 % forekommer i de fleste lærebøger inden for området. Nutidige data tyder dog på, at det nuværende tal er ca. 60 %. Uoverensstemmelsen mellem de traditionelle tal og de seneste undersøgelser skyldes det dramatiske fald i forekomsten af akut koronarsyndrom i løbet af de seneste årtier. Desuden er tidlig revaskularisering ved akutte koronare syndromer (STEMI, NSTEMI, ustabil angina) steget, hvilket har resulteret i færre hjertestop forårsaget af disse tilstande (Jerkeman et al).
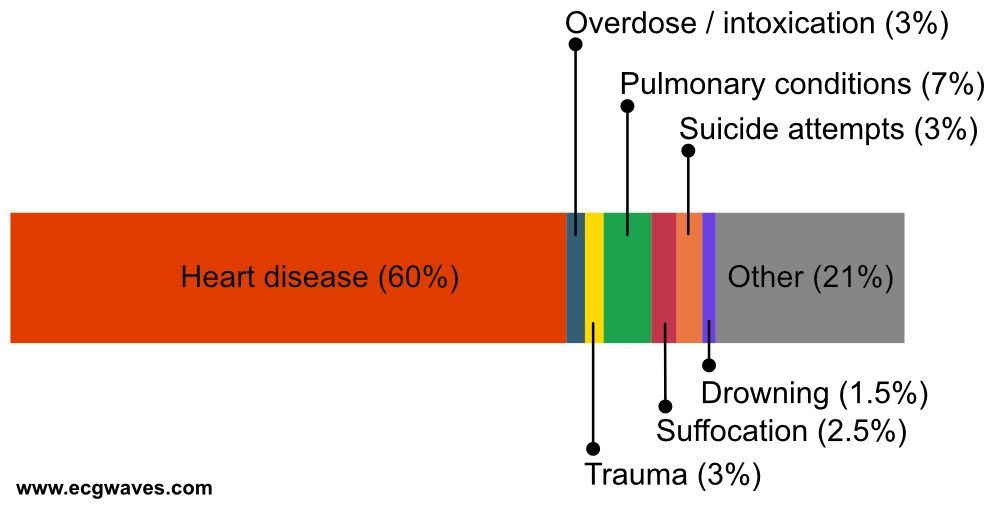
Det er ofte vanskeligt at fastslå årsagen til et hjertestop uden for hospital. Obduktion anbefales, når den underliggende årsag er ukendt, især blandt unge mennesker. Alligevel bliver obduktioner ofte ikke udført på grund af de høje omkostninger. Vanskelighederne ved at bestemme årsagen til hjertestop uden for hospital afspejles i den klassificering, der anbefales i henhold til Utstein-retningslinjerne (tabel 1). De brede kategorier af årsager anses for at være nødvendige på grund af den usikkerhed, der hersker i præhospitale omgivelser (Perkins et al.). Figur 1 viser data fra det svenske hjertestopregister, som har registreret årsager til hjertestop med en separat kategori for kardiale ætiologier.
| Årsag | Definition |
|---|---|
| Medicinsk årsag | Omfatter hjertestop forårsaget af hjertesygdom, andre medicinske tilstande (lungeemboli, blødning, slagtilfælde osv.) samt tilfælde, hvor årsagen ikke falder ind under de andre kategorier. |
| Traume | Hjertestop forårsaget af vold, ulykker, forbrændinger eller andre traumer. |
| Drukning | Hjertestop på grund af drukning |
| Elektrisk stød | Hjertestop på grund af elektrisk strøm gennem hjertet. |
| Asfyksi | Asfyksi som følge af ydre årsager, f.eks. fremmedlegeme, hængning eller kvælning. |
| Overdosering af medicin | Forsætlig eller utilsigtet overdosering af medicin, narkotika eller andre stoffer (herunder alkohol), der forårsager hjertestop. |
Kardial ætiologi
Hjertestop forårsaget af kardiovaskulære tilstande og hændelser er meget stokastiske begivenheder. Det skyldes, at langt størstedelen af disse anfald skyldes ventrikulære arytmier (ventrikulær takykardi, ventrikelflimmer), hvis forekomst er meget stokastisk. Dette fremgår tydeligt af det faktum, at langt størstedelen af alle myokardieinfarkter og episoder med myokardieiskæmi ikke forårsager ventrikulære arytmier og hjertestop. Det er klart, at kun en ubetydelig del af alle episoder med myokardieiskæmi resulterer i hjertestop. For at et infarkt eller en iskæmisk episode kan resultere i ventrikulær arytmi, skal det falde sammen med andre pro-arytmogene faktorer. Fremkomsten af ventrikulær takykardi eller ventrikelflimmer er derfor resultatet af et perfekt stormscenarie, hvor iskæmi, hæmodynamik, det autonome nervesystem, elektrolytkoncentrationer og andre faktorer (potentielt også genetisk disposition) interagerer for at udløse ventrikulær takykardi eller ventrikelflimmer. Disse faktorer interagerer og varierer over tid. Nogle faktorer varierer fra sekund til sekund (f.eks. graden af iskæmi, parasympatisk og sympatisk tonus), mens andre tager måneder eller år at udvikle (f.eks. myokardial remodellering ved hjertesvigt eller efter myokardieinfarkt).
Ventrikulære arytmier er lettere at fremkalde, hvis der er arytmogene substrater til stede. Et substrat defineres som en fysiologisk eller anatomisk faktor, der kan udløse eller opretholde arytmier, f.eks. nekrotisk væv efter et myokardieinfarkt (se Mekanismer for hjertearytmier).
Det er ofte vanskeligt at afklare den nøjagtige mekanisme, der forårsager hjertestop, selv om man kender et substrat. En patient med iskæmisk kardiomyopati kan have flere substrater – f.eks. nekrotisk væv i myokardiet, hjertesvigt med dilatation og remodellering af myokardiet og gentagne episoder med iskæmi på grund af stenoser i kranspulsårerne – hvilket gør det vanskeligt at bestemme den nøjagtige udløsende faktor.
Kroniske og akutte koronare syndromer
- Akut myokardieiskæmi kan fremkalde ventrikulær takykardi og ventrikelflimmer og dermed forårsage hjertestop. Dette kan forekomme på et hvilket som helst tidspunkt i det naturlige forløb af koronararteriesygdom, herunder som den første manifestation af koronar hjertesygdom. Arytmimekanismen er i de fleste tilfælde re-entry omkring den iskæmiske zone.
- Akut myokardieinfarkt kan også forårsage ventrikulær takykardi og ventrikelflimmer. Arytmimekanismen er også re-entry. Risikoen for ventrikulær takykardi og ventrikelflimmer er størst i løbet af de første minutter og den første time og aftager derefter hurtigt.
- Kroniske totale okklusioner (CTO) er komplette og kroniske okklusioner af kranspulsårerne. Stort set alle CTO’er har kollaterale kar (fra andre arterier), som reperfunderer den okkluderede arterie, så det udsatte myokardium kan perfunderes. Myokardiet vil dog sandsynligvis have udviklet arytmisubstrater (f.eks. infarkt) på trods af støtten fra kollaterale kar. Kollateraler kan forhindre eller begrænse yderligere infarkt og muliggøre fuld kontraktil funktion i hvile. Den funktionelle reserve i kollateraler er dog begrænset, og langt de fleste patienter med CTO’er oplever iskæmiske symptomer relateret til det myokardium, der forsynes af CTO’en. Nylige undersøgelser viser, at ca. 35 % af patienter med hjertestop uden for hospitalet med en indledende stødbar rytme har CTO’er (Lemkes et al.).
- Iskæmisk kardiomyopati. Iskæmisk kardiomyopati er kendetegnet ved remodellering, ardannelse og hjertesvigt, som udgør en meget høj risiko for maligne ventrikulære arytmier. Patienter med iskæmisk kardiomyopati har en høj risiko for pludseligt hjertestop.
Blandt patienter, der oplever hjertestop, er tidligere myokardieinfarkt betydeligt mere almindeligt end akut myokardieinfarkt. Et tidligere infarkt ses i 40-70 % af alle hjertestop uden for hospital, mens et akut eller nyligt infarkt ses i 20 % af tilfældene. I POST-SCD-undersøgelsen havde kun 30 % af alle tilfælde akut koronarsyndrom (Tseng et al.). Blandt tilfælde med koronararteriesygdom som underliggende årsag til hjertestop udgør gamle infarkter således størstedelen af substraterne.
Risikoen for hjertestop stiger med omfanget af iskæmien eller infarktet. Risikoen øges også med elektrolytubalance, hypotension, hypertension, belastning af venstre ventrikel og med sympatisk aktivering.
Andre årsager relateret til kranspulsårerne
- Medfødte anomalier i kranspulsårerne
- Medfødte varianter i udspringet af kranspulsårerne forekommer hos 5 % af alle individer (Angelini et al.). Nogle varianter er forbundet med en øget risiko for pludseligt hjertestop, især under anstrengende træning.
- Myokardiebroer (forekommer hos 1 % af befolkningen) menes at øge risikoen for pludseligt hjertestop, især under træning. Broer defineres som epikardiale segmenter af kranspulsåren, der løber inden for myokardiet, hvilket resulterer i kompression af kranspulsåresegmentet (figur 1).
- Emboli i kranspulsårerne
- Emboli fra endokarditis (aortaklap, mitralklap).
- Emboli fra tromber i den proksimale aorta.
- Emboli fra mural trombe i venstre ventrikel.
- Emboli fra tromber dannet i venstre atrial appendage.
- Arteritis (betændelse i kranspulsårerne)
- Kawasakis sygdom.
- Polyarteritis nodosa (PAN).
- Kranspulsårekrampe kan forårsage pludseligt hjertestop på grund af ventrikulære arytmier. Risikoen synes at være højere, hvis krampen opstår i aterosklerotiske kranspulsårer med stenoser.
- Proximal aortadissektion med okklusion af koronarostium kan føre til omfattende iskæmi og ventrikulære arytmier.

Troponin til differentialdiagnose af hjertestop
Hjertespecifikt Troponin T (TnT) og Troponin I (TnI) analyseres ofte i tilfælde af hjertestop uden for hospitalet for at afgøre, om hjertestoppet var forårsaget af et akut myokardieinfarkt. Rationalet bag dette er, at myokardienekrose begynder efter 20 minutters fuldstændig myokardieanoksi. Derfor bør hjertestop af andre årsager end akut myokardieinfarkt have lave troponinniveauer i modsætning til hjertestop forårsaget af infarkt, som bør resultere i høje troponinniveauer. Det er dog tvivlsomt, om troponin kan bruges til dette formål. I en undersøgelse af 145 patienter, der genvandt cirkulationen efter hjertestop og gennemgik serielle troponinmålinger og ekkokardiografiske undersøgelser, havde alle individer forhøjede troponinniveauer, og niveauerne kunne ikke bruges til at skelne infarktrelateret hjertestop fra andre årsager. Troponinniveauerne korrelerede heller ikke med overlevelse eller venstre ventrikelfunktion (Agusala et al.).
Foreslået læsning: Hjertetroponin I (TnI) og T (TnT): Fortolkning og evaluering ved akut koronarsyndrom
Hypertrofi og hypertrofisk kardiomyopati
Alle typer hypertrofi, uanset ætiologi og lokalisering, øger risikoen for ventrikulære arytmier og pludseligt hjertestop. Den mest almindelige årsag til ventrikelhypertrofi er arteriel hypertension, som resulterer i venstre ventrikelhypertrofi. Da hypertension også forårsager koronararteriesygdom, udviser disse personer ofte både hypertrofi og iskæmi, hvilket øger risikoen for arytmier. Risikofaktorer for åreforkalkning er stærkt forbundet med aortastenose, som også er almindelig blandt disse patienter. Den absolutte risiko for pludseligt hjertestop ved venstre ventrikelhypertrofi er dog lav.
Højre ventrikelhypertrofi er normalt et resultat af pulmonal hypertension. Disse patienter har også en øget risiko for pludseligt hjertestop.
Hypertrofisk kardiomyopati (HCM) er en genetisk kardiomyopati, der er defineret ved lokaliseret eller generaliseret venstre ventrikelhypertrofi. Hypertrofien er normalt lokaliseret (septal hypertrofi, apikal hypertrofi, lateral væghypertrofi). Ved septal hypertrofi kan der opstå obstruktion af LVOT (venstre ventrikels udstrømningskanal), hvilket resulterer i en tilstand, der kaldes hypertrofisk obstruktiv kardiomyopati (HOCM). HOCM er en af de mest almindelige årsager til pludseligt hjertestop hos unge mennesker, især atleter. Ved HOCM er pludseligt hjertestop sandsynligvis ikke forårsaget af udløbsobstruktionen, men snarere et resultat af ventrikulære arytmier.
Hypertrofi er, uanset ætiologi, en uafhængig risikofaktor for ventrikulære arytmier og pludseligt hjertestop. Risikoen for arytmier korrelerer med graden af hypertrofi, venstre ventrikels funktion (ejektionsfraktion) og ventrikelstørrelse. Nedsat ejektionsfraktion og ventrikeldilatation øger risikoen for pludseligt hjertestop.
Kardiomyopatier
Alle kardiomyopatier er forbundet med en øget risiko for pludselig hjertedød. Generelt er en historie med synkoper, familiehistorie med hjertestop eller pludselig hjertedød, tilbagevendende ventrikulære arytmier og tidlig debut af kardiomyopati forbundet med en høj risiko for pludseligt hjertestop. Hos patienter med kardiomyopati bør uforklarlige synkoper altid give anledning til mistanke om ventrikulær arytmi.
Blandt patienter med HFREF (hjertesvigt med reduceret ejektionsfraktion) dør ca. 50 % af pludseligt hjertestop (Packer et al.). Jo lavere ejektionsfraktion, jo højere er risikoen for pludseligt hjertestop. Langt størstedelen af de pludselige dødsfald ved hjertesvigt skyldes ventrikulære takyarytmier (ventrikulær takykardi, ventrikelflimmer). Et mindretal er forårsaget af bradyarytmier. Blandt patienter med HFPEF (hjertesvigt med bevaret ejektionsfraktion) dør ca. en tredjedel af pludseligt hjertestop (Vaduganathan et al.).
Iskæmisk kardiomyopati med hjertesvigt er forbundet med en markant øget risiko for pludseligt hjertestop, sandsynligvis mere end nogen anden kardiomyopati.
Andre typer kardiomyopati medfører også en øget risiko for pludseligt hjertestop:
- Dilateret kardiomyopati (DCM)
- Restriktiv kardiomyopati (RCM)
- Alkohol-kardiomyopati
- Diabetes-kardiomyopati
- Peripartum-kardiomyopati
Myokarditis er normalt en godartet tilstand, men den kan kompliceres af akut hjertesvigt, ventrikulære arytmier og hjertestop.
Arytmogen højre ventrikel-kardiomyopati (ARVC)
ARVC øger risikoen for ventrikulære arytmier (monomorf VT, polymorf VT, ventrikelflimmer) og pludselig hjertedød. Kardiomyopatien påvirker normalt den højre ventrikel, men kan også involvere den venstre ventrikel. Disse patienter bør ikke udsætte sig selv for anstrengende fysisk aktivitet. Synkope er en stærk prædiktor for fremtidig risiko for pludseligt hjertestop.
Akut hjertesvigt
Talrige tilstande, såsom akut myokardieinfarkt, akut-on-kronisk hjertesvigt, endokarditis, hypertensiv krise osv. kan forårsage akut hjertesvigt. Risikoen for pludseligt hjertestop er høj. Det skyldes ventrikulære arytmier og/eller kardiogent chok. Ved akut hjertesvigt er der en akut belastning på venstre ventrikel sammen med en kraftig sympatisk respons og potentielt andre faktorer, der øger risikoen for arytmier.
Inflammatoriske årsager og lagringssygdomme
- Kæmpecelle-myokarditis medfører en høj risiko for hjertestop.
- Eosinofil myokarditis medfører også en høj risiko for hjertestop.
- Hjertepåvirkning forekommer hos 20 % af personer med sarkoidose, og halvdelen af disse oplever hjertesymptomer (Ekström et al.). Ventrikulær takykardi er almindelig, og risikoen for hjertestop er betydeligt forøget.
- Systemisk sklerose (sklerodermi) medfører også en øget risiko for hjertestop.
- Amyloidose (AL, ATTR) øger også risikoen for hjertestop.
Valvulær hjertesygdom
Venstresidige valvulære læsioner er klart forbundet med pludseligt hjertestop, især aortastenose, som medfører en årlig risiko på 1 % for pludseligt hjertestop. Risikoen stiger med sværhedsgraden af aortastenose, men kan halveres ved indgreb (kirurgisk klapudskiftning eller TAVI). Der er dog fortsat en øget risiko, selv efter indgrebet, hvilket kan forklarees med sameksisterende koronararteriesygdom, hjertesvigt, hypertrofi og protesedysfunktion.
Både kirurgiske indgreb og TAVI kan forårsage højgradig AV-blok, men pludseligt hjertestop er en sjælden komplikation, da disse patienter EKG-overvåges i flere dage.
Prolaps af mitralklappen er også forbundet med en øget risiko for pludseligt hjertestop. En variant kaldet mitral annular disjunction (MAD) kan være forbundet med en højere risiko for hjertestop, selvom den videnskabelige evidens er begrænset (Bennett et al.).
Aortaregurgitation og mitralregurgitation medfører en let øget risiko for pludseligt hjertestop.
Endokarditis
Endokarditis fører sjældent til ventrikulære arytmier. Tilstedeværelsen af sådanne arytmier bør give mistanke om septisk emboli i kranspulsårerne, som kan forårsage ventrikulære arytmier (VT, VF).
Medfødt hjertesygdom
Medfødte hjertesygdomme, der øger risikoen for pludseligt hjertestop, omfatter:
- Medfødt aortastenose
- Shunts, der øger den pulmonale vaskulære modstand (PVR)
- Eisenmengers syndrom
- Fallots tetralogi
- Transposition af de store arterier
- Defekter i AV-kanalen
Efter korrigerende kirurgi kan arvæv resultere i ventrikulære arytmier og pludselig hjertestop.
Ledningsdefekter (AV-blok)
AV-blok er en mindre almindelig årsag til pludseligt hjertestop. Det skyldes hjertets pacemakerhierarki. Fejl i sinusknuden fører næsten altid til, at der opstår en flugtrytme med oprindelse i atrierne, AV-knuden, His-Purkinje-systemet eller det ventrikulære myokardium, i nævnte rækkefølge. Men flugtrytmer er ikke pålidelige på lang sigt, da de kan svigte når som helst. AV-blokke af høj grad skal derfor betragtes som potentielt livstruende, selv hvis der er en tilsyneladende stabil flugt-rytme til stede. Højgradig AV-blok behandles med atropin og/eller isoproterenol eller en midlertidig pacemaker, indtil et permanent system er implanteret (hvis det er nødvendigt).
Bemærk, at AV-blok 1 og AV-blok 2 type 1 kan udvikle sig til højgradig AV-blok (AV-blok 2 type 2, AV-blok 3). Risikoen anses dog for at være meget lav ved AV-blok 1 og lav ved AV-blok 2 type 1. Myokardieinfarkt kompliceret af højre grenblok og fascikulært blok indikerer en øget risiko for komplet AV-blok.
Intraventrikulære ledningsdefekter med brede QRS-komplekser indikerer en øget risiko for pludseligt hjertestop blandt patienter med koronararteriesygdom. Tilstedeværelsen af patologiske Q-bølger indikerer et tidligere stort myokardieinfarkt, som udgør et betydeligt substrat for maligne ventrikulære arytmier (VT, VF).
Præeksitation (Wolff-Parkinson-White syndrom, WPW) kan forårsage hæmodynamisk signifikante takyarytmier (ortodrom AVRT, antidrom AVRT), men meget sjældent pludseligt hjertestop. Alligevel bør risikoen for pludseligt hjertestop betragtes som høj blandt patienter, hvis accessoriske vej har en kort anterograd refraktærperiode (dvs. kan lede impulser fra atriet til ventriklen med en kort refraktærperiode), da atrieflimren hos disse patienter kan overføres til ventrikelflimren (VF) og dermed forårsage pludseligt hjertestop.
Lang QT-syndrom (LQTS)
Forlængelse af QT-intervallet kan fremkalde torsades de pointes ventrikulær takykardi, som kan være selvterminerende (ophøre spontant), men der er stor risiko for progression til ventrikelflimmer. Torsade de pointes bør betragtes som en meget ustabil arytmi. Størstedelen af personer med forlænget QT-interval har fået det som følge af bivirkninger af medicin (se nedenfor). Medfødt forlængelse af QT-intervallet er langt mindre almindeligt. De karakteristiske EKG-forandringer ved medfødt LQTS type 1, 2 og 3 er vist nedenfor. Uanset årsagen til torsades de pointes er der stor risiko for ventrikelflimmer.
Medfødt LQTS (langt QT-syndrom)
Langt QT-syndrom (LQTS) er en forstyrrelse af hjertets repolarisering, der er kendetegnet ved et forlænget QT-interval, som øger risikoen for ventrikulære arytmier og pludseligt hjertestop. LQTS er en heterogen lidelse med forskellige genetiske mutationer, der forårsager lidelsen.
LQTS type 1 (LQT1) er den mest almindelige form for medfødt LQTS og skyldes en mutation i KCNQ1-genet, som resulterer i et tab af funktion af hjertets kaliumkanal. Arytmier opstår typisk under fysisk anstrengelse, især svømning, og andre sympatiske udløsere. EKG-fundene omfatter bredt baserede T-bølger.
LQTS type 2 (LQT2) skyldes en mutation i KCNH2-genet, som også fører til et tab af kaliumkanalens funktion. Arytmier opstår typisk ved pludselige overraskelser (f.eks. høje lyde eller frygt), stress, fysisk anstrengelse eller under søvn. EKG-fundene ved LQT2 omfatter en T-bølge med lav amplitude og en ekstra pukkel eller et ekstra hak. Efter fødslen er der risiko for torsades de pointes høj.
LQTS type 3 (LQT3) er forårsaget af en mutation i SCN5A-genet, som fører til øget natriumindstrømning. Pludselig død under søvn er typisk, og bradyarytmier kan også give anledning til maligne arytmier. EKG-fundene ved LQT3 omfatter en sen start af T-bølgen (med et langt og tydeligt ST-segment) og en spids T-bølge.
LQTS type 4 (LQT4) er sjælden og udgør kun 1 % af tilfældene. Den skyldes en mutation i ANKB-genet, som koder for et protein, der forankrer membranproteiner til cytoskelettet. LQT4 kan forårsage forskellige arytmier, f.eks. familiær katekolaminerg polymorf ventrikulær takykardi, atrieflimren, ledningsforstyrrelser, sinusknudedysfunktion og bradykardi.
Andre varianter af LQTS er meget sjældne og ofte en del af mere omfattende syndromer, der involverer flere organsystemer (Jervell og Lange-Nielsens syndrom, Romano-Wards syndrom). Patienter med medfødt LQTS bør ikke bruge lægemidler, der forlænger QT-intervallet (se nedenfor).
Det er vanskeligt at forudsige risikoen for hjertestop ved LQTS. Nogle personer oplever aldrig arytmier, mens andre har gentagne hjertestop. Følgende er risikofaktorer eller advarselstegn for hjertestop ved LQTS:
- Synkope
- Markant forlænget QT-interval
- QT alternans (varierende QTc-interval)
- Familiehistorie med pludselig hjertedød
- Forekomst af torsade de pointes, anden ventrikulær takykardi, ventrikelflimmer
Erhvervet LQTS
Mange tilstande og lægemidler kan fremkalde QT-forlængelse, hvilket fører til erhvervet LQTS. Denne type LQTS er mere almindelig end den medfødte form. Medicinske tilstande, situationer og lægemidler, der kan forårsage eller forværre LQTS, omtales i Liste over lægemidler og tilstande, der forårsager langt QT-syndrom.
Kort QT-syndrom (SQTS)
SQTS er en sjælden tilstand, der er kendetegnet ved et QTc-interval <300 ms, hvilket også øger risikoen for ventrikulære arytmier og hjertestop.
J-bølge-syndromer
Der er to J-bølgesyndromer, som øger risikoen for hjertestop, nemlig Brugadas syndrom og Early Repolarization Syndrome.
Brugadas syndrom
Brugadas syndrom er en autosomal dominant arvelig tilstand. Der er 12 kendte genmutationer, som påvirker transporten af natrium eller calcium over cellemembranen. Personen er normalt asymptomatisk indtil 20-55 års alderen og præsenterer sig med synkope, ventrikelflimmer, ventrikulær takykardi, hjertestop og/eller pludselig hjertedød. Da syndromet er arveligt, er der ofte en familiehistorie med synkoper og uventede hjertestop. De karakteristiske EKG-forandringer er intermitterende. EKG-forandringer og arytmier ser ud til at forekomme hyppigere i hvile, under søvn, ved feber og i situationer med høj vagal tone. Fysisk anstrengelse ser ikke ud til at øge risikoen for arytmier. Mænd er overrepræsenteret blandt dem, der får hjertestop, og det samme er tilfældet med Brugadas syndrom type 1. EKG-forandringer og arytmier kan fremkaldes med ajmalin, flecainid og procainamid.
Typer af Brugada-syndrom
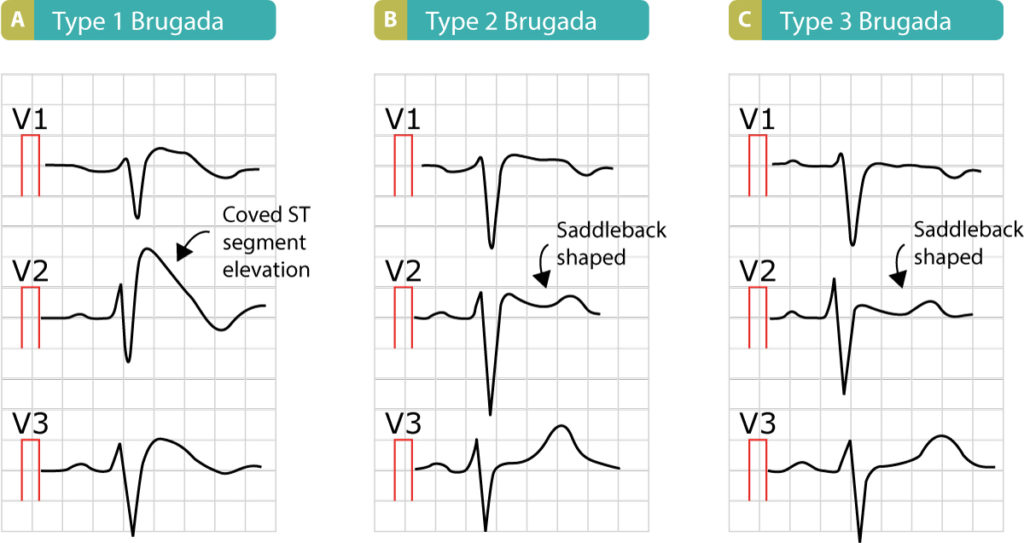
Brugadas syndrom type 1 er kendetegnet ved en kileformet ST-segmentforhøjelse ≥2 mm, som overgår til en negativ T-bølge. Hvis dette mønster er til stede i afledning V1 og/eller V2, er diagnosen bekræftet. Brugadas syndrom type 2 er karakteriseret ved en sadelrygformet ST-segmentforhøjelse med et forhøjet J-punkt ≥2 mm. Den terminale del af ST-segmentet er forhøjet ≥1 mm. Type 3 Brugada-syndrom ligner type 2, men den terminale del af ST-segmentet er forhøjet <1 mm.
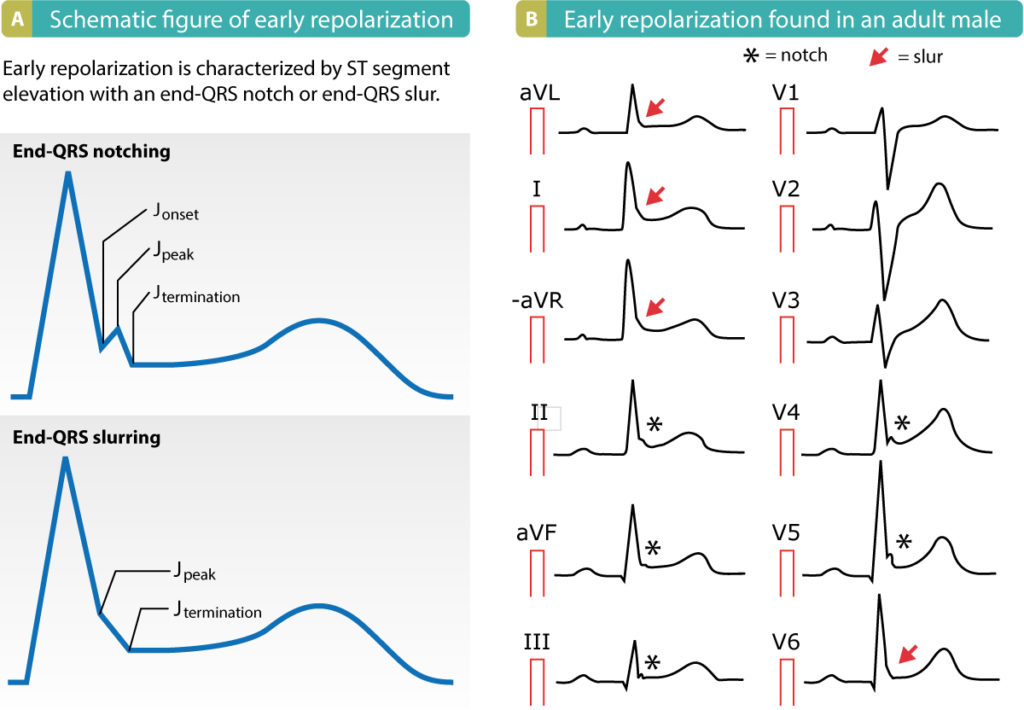
Syndrom med tidlig repolarisering
Ca. 5-13 % af befolkningen udviser tidlig repolarisering på EKG’et (70 % af dem er mænd). Tidlig repolarisering, især i afledning II, aVF og III, er forbundet med idiopatisk ventrikelflimmer og en 3-5 gange øget risiko for hjertestop. Selv om den relative risiko for hjertestop er høj sammenlignet med personer uden tidlig repolarisering, er den absolutte risiko meget lav.
ST-forhøjelserne har normalt et konkavt ST-segment og er mest udtalt i brystafledningerne. T-bølgerne er høje. Det vigtigste fund er tilstedeværelsen af en pukkel eller hældning ved overgangen fra R-bølgen til ST-segmentet (se figur). Pukkelen ligger helt over basislinjen, og hældningen begynder, før basislinjen nås.
EKG-mønsteret betragtes som godartet, hvis det forekommer i de forreste brystafledninger (V3-V4). Jo højere J-punkterne er, desto større er risikoen for ventrikelflimmer. Det er sandsynligt, at tidlig repolarisering er en prædisponerende faktor for ventrikulære arytmier i situationer, der kan udløse sådanne arytmier, såsom myokardieiskæmi og myokardieinfarkt.
Katekolaminerg polymorf ventrikulær takykardi (CPVT)
Catecholaminerg polymorf ventrikulær takykardi (CPVT) er en arvelig tilstand med høj dødelighed på grund af pludselig hjertedød. Udbredelsen i befolkningen er ca. 1 ud af 10.000 individer. Der er en høj risiko for polymorf og tovejs VT. Ventrikulær takykardi er forårsaget af katekolaminer, hvilket gør betablokkere til en effektiv behandling. Hvile-EKG’et er typisk helt normalt.
Takotsubo-kardiomyopati
Takotsubo-kardiomyopati menes at være forårsaget af en ekstrem katekolaminerg bølge, der fører til udbredt myokardiebedøvelse, typisk lokaliseret til apex, som bliver ballonneret og midlertidigt mister kontraktilitet. Prognosen er generelt god, og det er uklart, om tilstanden er forbundet med en øget risiko for pludseligt hjertestop. Det kan forårsage QT-forlængelse. Dødeligheden øges primært på grund af hæmodynamisk kollaps snarere end ventrikulære arytmier.
Pludselig spædbarnsdød (SIDS)
Pludselig spædbarnsdød (SIDS) defineres som et uventet dødsfald mellem fødslen og 6-måneders-alderen. Det var mere almindeligt tidligere, da spædbørn sov på maven, men det frarådes nu, hvilket har resulteret i en halvering af forekomsten af SIDS. Mekanismen menes at være obstruktiv søvnapnø, men en del af disse spædbørn kan have LQTS.
Pludseligt hjertestop under sport og fysisk aktivitet
Sport og fysisk aktivitet er forbundet med en let øget risiko for akut myokardieinfarkt og pludseligt hjertestop under og efter fysisk aktivitet. Risikoen for pludseligt hjertestop under sport er ekstremt lav. Hos unge personer bør kardiomyopatier (HCM, HOCM, ARVD/ARVC, myokarditis) mistænkes i tilfælde af uforklarlig synkope eller pludseligt hjertestop. Mindre hyppigt kan ionkanalforstyrrelser og Brugadas syndrom være årsagen. Hos midaldrende og ældre personer er koronararteriesygdom den mest almindelige årsag. Efter myokarditis er fysisk aktivitet forbudt i 3 til 6 måneder, fordi risikoen for ventrikulære arytmier er størst i denne periode.
Andre årsager til hjertestop
- Andre årsager til hjertestop omfatter commotio cordis (traume mod brystkassen kan forårsage ventrikulær takykardi og ventrikelflimren).
- Ondartet hypertermi, bl.a. under fysisk anstrengelse i varme.
- Idiopatisk VF (ventrikelflimmer uden underliggende årsag).
- Lungeemboli.
- Luftemboli.
- Søvnapnø forårsager hjertestop via apnø.
- Dissektion af aorta.
- Tamponade.
Referencer
Sadie Bennett, Ritu Thamman, Timothy Griffiths, Cheryl Oxley, Jamal Nasir Khan, Thanh Phan, Ashish Patwala, Grant Heatlie, Chun Shing Kwok. Mitral annular disjunction: En systematisk gennemgang af litteraturen Sadie Bennett. Ekkokardiografi . 2019 Aug;36 (8):1549-1558.
Vaduganathan M, Patel R.B, Michel A, et al. Dødsmåde ved hjertesvigt med bevaret ejektionsfraktion. J Am Coll Cardiol . 2017;69:556-569.
Ekstrom K, Lehtonen J, Nordenswan H.K, et al. Sudden death in cardiac sarcoidosis: an analysis of nationwide clinical and cause-of-death registries. Eur Heart J . 2019;40:3121-3128.
Finocchiaro G, Papadakis M, Robertus J.L, et al. Ætiologi af pludselig død i sport: indsigt fra et regionalt register i Storbritannien. J Am Coll Cardiol . 2016;67:2108-2115.
Minners J, Rossebo A, Chambers J.B, et al. Pludselig hjertedød hos asymptomatiske patienter med aortastenose. Heart . 2020;106:1646-1650
Urena M, Webb J.G, Eltchaninoff H, et al. Late cardiac death in patients undergoing transcatheter aortic valve replacement: incidence and predictors of advanced heart failure and sudden cardiac death. J Am Coll Cardiol . 2015;65:437-448.
Fulton B.L, Liang J.J, Enriquez A, et al. Billeddannelseskarakteristika for papillarmusklens oprindelsessted for ventrikulære arytmier hos patienter med mitralklap-prolaps. J Cardiovasc Electrophysiol . 2018;29:146-153.
Myerburg R.J. Fysiologiske variationer, miljøfaktorer og genetiske modifikationer i arvelige LQT-syndromer. J Am Coll Cardiol . 2015;65:375-377.
Sollazzo F, Palmieri V, Gervasi S.F, et al. Pludselig hjertedød hos atleter i Italien i løbet af 2019: Internetbaseret epidemiologisk forskning. Medicina (Kaunas) . 2021;57.
Tseng Z.H, Olgin J.E, Vittinghoff E, et al. Prospective countywide surveillance and autopsy characterization of sudden cardiac death: post scd study. Cirkulation . 2018;137:2689-2700.
Coronary Artery Anomalies An Entity in Search of an Identity Paolo Angelini Oprindeligt udgivet13. marts 2007https://doi.org/10.1161/CIRCULATIONAHA.106.618082. Circulation. 2007;115:1296-1305
