Avanceret kardiopulmonal genoplivning (HLR) – Avanceret kardiovaskulær livsstøtte (ACLS)
Dette kapitel omhandler interventioner og evalueringer, der udføres under avanceret kardiovaskulær genoplivning (ACLS). Mens basal genoplivning (BLS) kan udføres af stort set alle, udføres avanceret kardiopulmonal genoplivning (ACLS) af sundhedspersonale med de nødvendige færdigheder og det nødvendige udstyr. Selvom ACLS er mere avanceret og dyrere end de interventioner, der er tilgængelige i BLS, er antallet, der skal behandles (NNT) for de ACLS-specifikke interventioner, meget højere eller usikkert, hvilket betyder, at effekten af disse interventioner er meget lavere eller usikker. De største muligheder for overlevelse findes faktisk i løbet af de første par minutter efter kollapset. Tabel 1 viser number needed to treat (NNT) for forskellige interventioner, der indgår i BLS og ACLS.
| Intervention | BLS eller ACLS | NNT for at redde 1 person | Reference |
|---|---|---|---|
| Tidlig opdagelse af hjertestop | BLS | 11 | Berdowski et al |
| HLR for tilskuere | BLS | 15 | Hasselqvist et al |
| Tidlig defibrillering | BLS (hvis AED er tilgængelig) | 5 | Kitamura et al |
| Adrenalin (epinefrin) | ACLS | 112 | Perkins et al |
| Avanceret luftvej | ACLS | Uklar fordel | Panchal et al |
| Trakeal intubation vs. bag-mask ventilation | ACLS | Uklar fordel | Jabre et al |
| Mekaniske kompressioner | ACLS | Ingen fordel | Rubertsson et al |
| Amiodaron, Lidokain | ACLS | Uklar fordel | Kudenchuk et al |
| ECMO | ACLS | Ingen fordel | Suverein et al |
| Målrettet temperaturstyring | ACLS, | Ingen fordel | Dankiewicz et al |
| Ekkokardiografi | ACLS | Ingen fordel | Panchal et al |
Number Needed to Treat (NNT) er det antal patienter, der skal behandles for at redde én. Hvis en intervention har en NNT på 10, skal der behandles 10 personer for at redde 1.
AED = automatisk ekstern defibrillator. ECMO = Ekstrakorporeal membranoxygenering. ALS = avanceret livsstøtte.
Avanceret hjerte-lunge-redning (ACLS) bør iværksættes så tidligt som muligt. Ved hjertestop uden for hospitalet (OHCA) udføres ACLS af paramedicinere, sygeplejersker eller læger, afhængigt af det præhospitale systems udformning. ACLS indebærer anlæggelse af en avanceret luftvej, defibrillering af stødbare rytmer, administration af antiarytmika, overvejelse af målrettede indgreb (f.eks. transkutan pacing), revurdering af prognosen og bestemmelse af, om der er behov for yderligere indgreb eller undersøgelser.
Retningslinjer for hjertestop på hospitaler anbefaler, at HLR starter med det samme, og at defibrillering udføres inden for 180 sekunder (for stødbare rytmer) efter bekræftet hjertestop.
Hvis det ikke er muligt at give effektiv HLR på grund af offerets position, er det nødvendigt at flytte offeret til en position, hvor HLR kan udføres på passende vis (f.eks. en hurtig overflade).
Luftveje
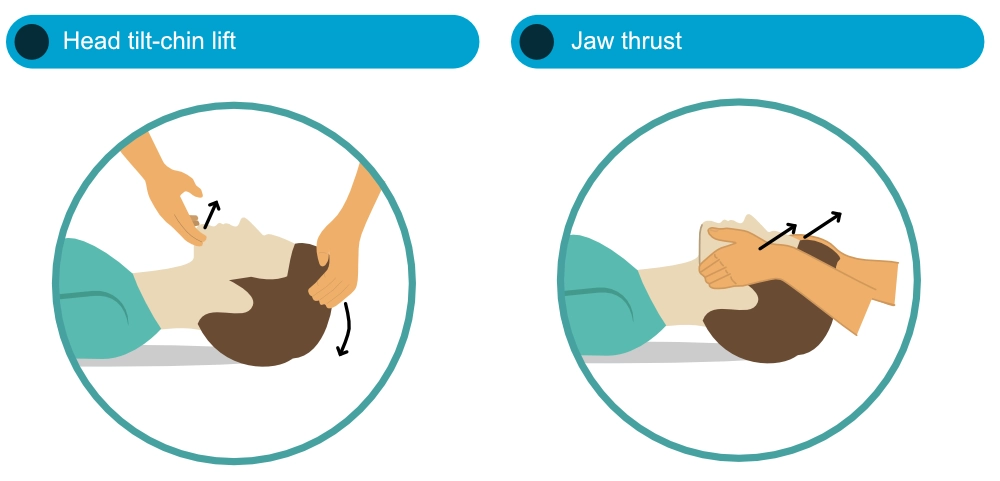
Metoden med at vippe hovedet og løfte hagen er effektiv til at åbne luftvejene. Den optimale metode til at åbne luftvejene er dog stadig ukendt (Guildner et al.). Kæbestød er at foretrække, hvis der er mistanke om skader på halshvirvelsøjlen, og i så fald bør hoved-kæbeløft kun anvendes, hvis andre metoder ikke kan åbne luftvejene.
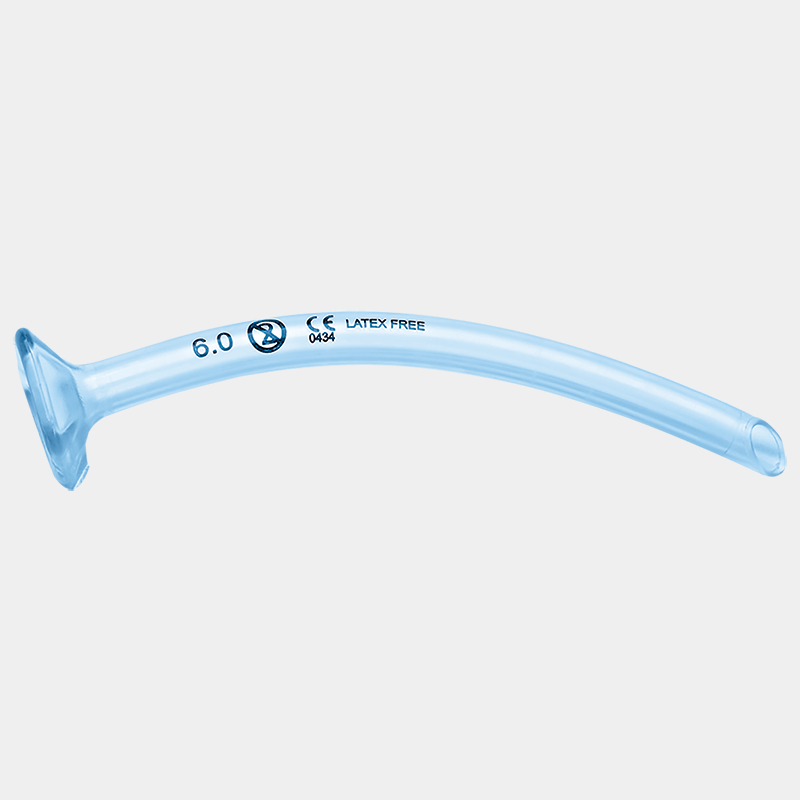
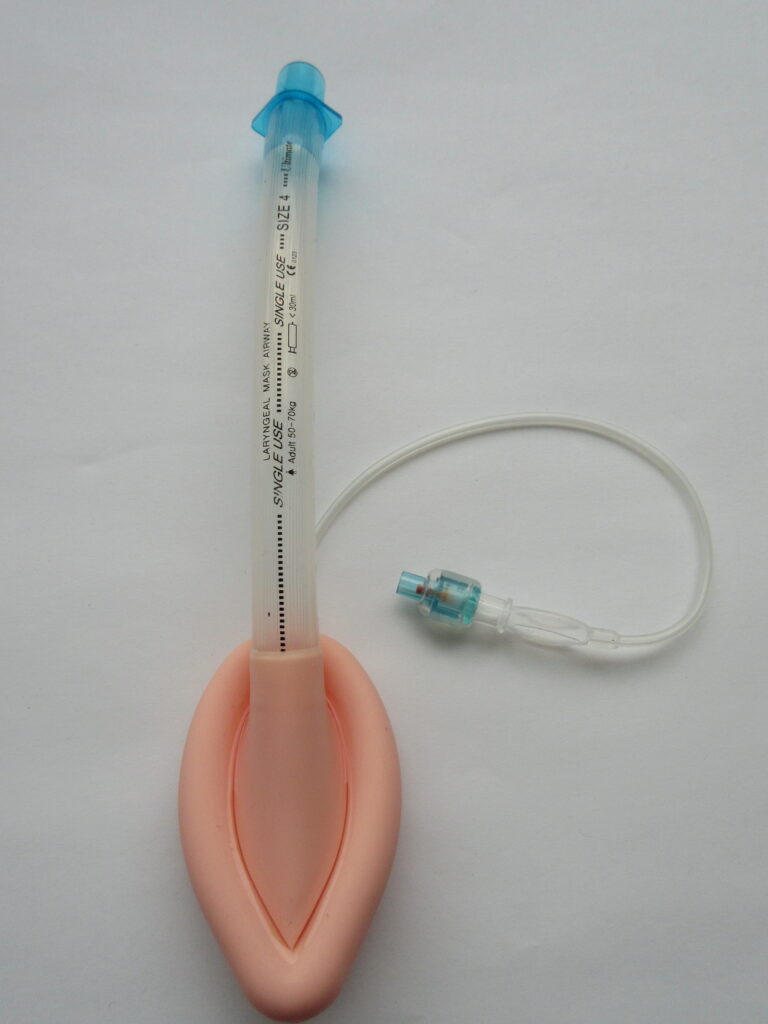
Ingen store undersøgelser har sammenlignet orofaryngeale og nasofaryngeale luftveje ved hjertestop. Endotrakeal (trakeal) intubation anses for at være den mest pålidelige luftvej, forudsat at den placeres af erfarent personale. En supraglottisk luftvej er et rimeligt alternativ, hvis der ikke kan etableres en trakealtube. Nasofaryngeale luftveje kan forårsage komplikationer hos patienter med kraniebrud (risiko for intrakraniel fejlplacering af tuben) eller koagulopati (risiko for blødning).
- En avanceret luftvej (trakealtube, supraglottisk luftvej) bør etableres så tidligt som muligt.
- Luftvejshåndtering bør ikke afbryde kompressioner i mere end 5 sekunder.
- Effekten af cricoid-tryk og gastrisk insufflation er stadig usikker (Panchal et al.).
- Nasofaryngeale luftveje (“trompeter”) skal indsættes omhyggeligt. Risikoen for epistaxis (næseblod) er betydelig og kan gøre luftvejshåndteringen vanskeligere.
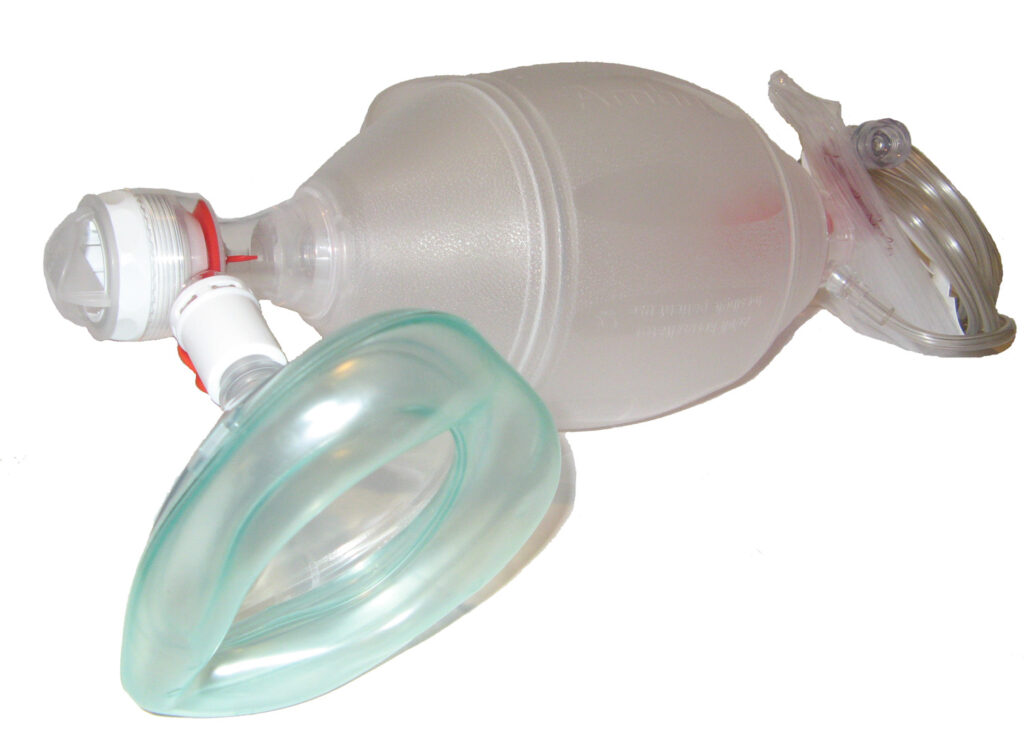


Ventilation
Ventilation kan udføres ved hjælp af mund-til-mund-åndedræt, bag-mask-ventilation eller respirator. Mund-til-mund-ventilation bruges kun i ACLS, hvis andre midler ikke er tilgængelige. Effektiv ventilation kan kræve gentagne justeringer af luftvejene og luftvejshjælpemidlet.
Når der er etableret en avanceret luftvej, fortsætter ventilation og kompression asynkront (dvs. kompressioner afbrydes ikke af ventilationer).
- Ventilér med 10 indblæsninger/min (1 indblæsning pr. 6 sekunder).
- der anvendes 100 % ilt (O2).
- Hvert åndedrag giver over 1 sekund.
- Tidevandsvolumen skal være 500-600 ml og give synlige brysthævninger.
- Placeringen af en trakealtube kan bekræftes ved hjælp af kapnografi (kapitel Kapnografi (ETCO2) ved hjertestop og genoplivning).
- Luftvejenes åbenhed skal løbende revurderes.
Hvis det ikke er muligt at placere en avanceret luftvej (trakealtube, supraglottisk luftvej), kan der anvendes bag-mask-ventilation eller regelmæssige indblæsninger.
Overdreven ventilation resulterer i overinflation, unødvendig stigning i det intrathorakale tryk og efterfølgende nedsat venøs tilbagestrømning og reduceret minutvolumen (Aufderheide et al.).
Kompressioner på brystet
Kompressionsfraktion
Kompressionsfraktionen, dvs. den samlede fraktion af HLR-tiden, der bruges på at udføre kompressioner, bør være mindst 60 %. Undersøgelser viser, at en højere kompressionsfraktion er forbundet med bedre resultater ved OHCA, uanset den oprindelige rytme (Vaillancourt et al., Talikowska et al.). Observationsdata fra Resuscitation Outcomes Consortium Investigators viste en 3 gange højere sandsynlighed for at blive udskrevet i live for patienter i den højeste kvintil (for kompressionsfraktion) og en 2 gange højere sandsynlighed for tilfælde i den næsthøjeste kvintil sammenlignet med den laveste. Sandsynligheden for overlevelse steg med 11 % for hver 10 % stigning i kompressionsfraktion (Christenson et al.).
Kompressionsfraktionen bør være mindst 60 %
Offerets position
Offeret skal ligge på ryggen på et hurtigt underlag under HLR. Der er ingen evidens for, at kompressioner er mindre effektive på sengemadrasser. Der er heller ingen evidens for, at backboards, som placeres mellem madrassen og patientens ryg, påvirker resultaterne. En systematisk gennemgang og metaanalyse af Paganini et al. viste, at rygbrædder øgede kompressionsdybden med 1,46 mm (0,057 tommer), hvilket sandsynligvis ikke påvirker overlevelsen.
Udførelse af manuelle brystkompressioner
- Håndfladen på den ene hånd placeres på den nederste halvdel af brystbenet, og den anden hånd placeres oven på den første hånd.
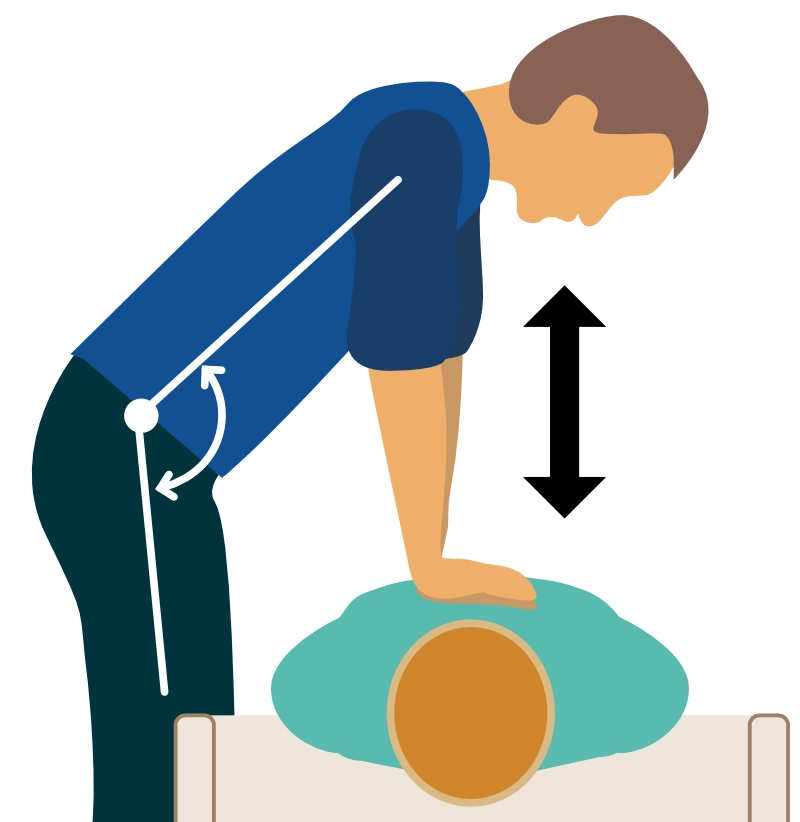
- Kompressoren (dvs. den person, der udfører kompressioner) skal bruge ryg- og overkropsmuskler til at udføre kompressionsarbejdet (figur 3). Brystbenet trykkes ned med strakte arme. Albuerne må ikke være bøjede.
- Kompressionshastigheden bør være 100 til 120 kompressioner pr. minut. Højere kompressionshastighed resulterer i mindre kompressionsdybde, hvilket sandsynligvis vil være skadeligt.
- Brystbenet skal trykkes ned 5,0-6,0 cm (2,0-2,4 tommer).
- Brystet skal frigøres hurtigt og fuldstændigt (dekompression) efter hver kompression. Fuld rekyl af brystet er vigtigt. Resterende lænet brystkasse forringer det koronare perfusionstryk.
- Skift kompressor hvertandet minut for at opretholde den ønskede kompressionsdybde. Undersøgelser har vist, at mens kompressionshastigheden opretholdes (eller endda øges) over 120 sekunder, mindskes kompressionsdybden med 2 mm (0,08 tommer) pr. minut (Sugerman et al).
Forholdet mellem kompression og ventilation
Kompressions-ventilationsforholdet er forholdet mellem kompressioner og ventilationer. Kompressions-ventilationsforholdet i basal livredning (BLS) er som følger (Kleinman et al):
- Voksne: 30:2 (30 kompressioner efterfulgt af 2 ventilationer).
- Spædbørn og børn med én redningsmand: 30:2.
- Spædbørn og børn med to redningsmænd: 15:2.
Kompressioner sættes på pause for at give indblæsninger i BLS. Efter etablering af en avanceret luftvej (supraglottisk luftvej [SGA] eller endotrakeal tube) kan kompressioner leveres uden pauser til ventilation (Jabre et al.).
Kompressioner fortsætter uafbrudt i ACLS, efter at en avanceret luftvej er blevet placeret.
Pre-shock og post-shock pause
Forsinkelser og afbrydelser i HLR (kompressioner) før eller efter defibrillering er forbundet med lavere ROSC og overlevelse (Tang et al, Steen et al, Rea et al, Bobrow et al).
- Pausen før og efter defibrillering skal være minimal.
- Pauser til rytme- og pulskontrol må ikke overstige 10 sekunder, og kompressionerne skal genoptages, når der ikke bekræftes en puls.
- Kompressioner genoptages altid umiddelbart efter defibrillering. Puls- og rytmekontrol vurderes under næste kontrol.
I ACLS er afbrydelser tilladt for rytme-/pulskontrol og defibrillering. Det anbefales, at defibrillatorer oplades, mens man afventer rytmetjekket, så stødbare rytmer kan defibrilleres uden forsinkelse.
Mekanismer, der driver hjertets udgang
Kapitlet Fysiologi ved hjerte-lunge-redning dykker ned i de fysiologiske mekanismer bag, hvordan brystkompressioner genererer hjertets minutvolumen. Kort fortalt forårsager kompression og dekompression af brystvariationer i det intrathorakale tryk. I dekompressionsfasen gør det lave tryk i højre atrium det muligt for blodet at strømme passivt til højre atrium og højre ventrikel. Omvendt øges hele det intrathorakale tryk i kompressionsfasen, hvilket fører til øget tryk i alle væv og kamre. Forudsat at klapperne fungerer normalt, sprøjtes blodet ud i anterograd retning mod aorta og dermed koronar- og hjernearterierne. Hjertet kan kun genstartes, hvis den koronare blodgennemstrømning er tilstrækkelig. Det koronare perfusionstryk (CPP) skal være mindst 15 mmHg for at fremkalde hjertets elektriske aktivitet, som er en forudsætning for hjertets mekaniske funktion og for at opnå ROSC (return of spontaneous circulation). Jo større det koronare perfusionstryk er, desto større er sandsynligheden for at fremkalde elektrisk aktivitet og få defibrilleret ventrikulær takykardi eller ventrikelflimmer (Ewy et al.). Afbrydelse af kompressioner har en øjeblikkelig og skadelig indvirkning på det koronare perfusionstryk, som det tager mange værdifulde sekunder at genopbygge.
HLR kun med kompressioner (håndholdt HLR)
HLR med kun kompressioner (hands-only CPR, compression-only CPR) svarer måske til standard HLR i BLS ved hjertestop uden for hospital (Jerkemean et al, Riva et al). HLR med kun kompressioner bruges dog ikke i ACLS og bør ikke bruges af sundhedspersonale, der giver BLS. Ventilation udføres altid i ACLS og af sundhedspersonale, der udfører BLS. De fysiologiske effekter diskuteres i kapitlet Fysiologi ved hjerte-lunge-redning.
Mekaniske kompressioner (MCPR, mekanisk HLR)
Mekanisk HLR kræver udstyr, der udfører kompressioner ved hjælp af batteristrøm. Eksempler på sådanne apparater er LUCAS, AutoPulse, Lifeline ARM og CorPuls (figur 4A-3D). Undersøgelser har ikke påvist nogen overlegenhed blandt disse apparater eller nogen overlevelsesfordel sammenlignet med manuel HLR. Mekanisk HLR anbefaler hund under ambulancetransport, i kateteriseringslaboratoriet og i andre situationer, hvor det er vanskeligt at udføre manuelle kompressioner af høj kvalitet.
Med hensyn til effektiviteten af disse apparater kan følgende undersøgelser nævnes:
- AutoPulse resulterede i en tre gange højere overlevelsesrate ved hjertestop uden for hospital (18,8 % vs. 6,3 %, p = 0,03), men ingen forskel i neurologisk funktion blandt de overlevende, og AutoPulse kan potentielt forårsage mere organskade (Koster et al, Gao et al).
- LUCAS påvirkede ikke overlevelsen i et stort randomiseret forsøg med OHCA (Rubertsson et al).
- I alt 6 systematiske gennemgange og metaanalyser har undersøgt mekanisk HLR, og der er ingen indikation af, at mekaniske kompressioner påvirker overlevelsen (Liu et al, Gates et al), selvom en undersøgelse indikerede øget overlevelse med mekaniske kompressioner ved hjertestop på hospitalet (Couper etal).
- LUCAS er muligvis mere effektiv end AutoPulse (Khan et al).
På grund af den iboende umulighed af at bruge blinding i disse forsøg skal alle resultater fortolkes med forsigtighed (Redberg et al.).
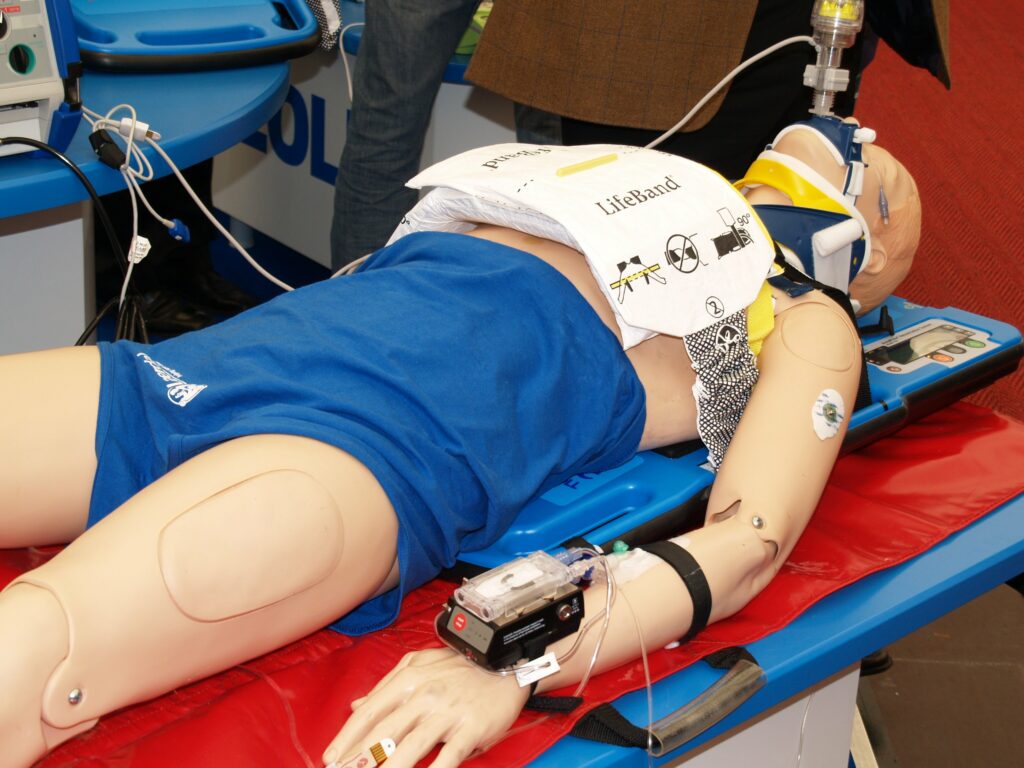



Videoinstruktioner til LUCAS, AutoPulse, Lifeline ARM og CorPuls følger nedenfor. Bemærk, at disse videoer er produceret af producenterne.
- Corpuls 3 & Corpuls HLR
- AutoPulse
- Physio-Control LUCAS 3 brystkompressionssystem
- Defibtech Lifeline ARM
Defibrillering
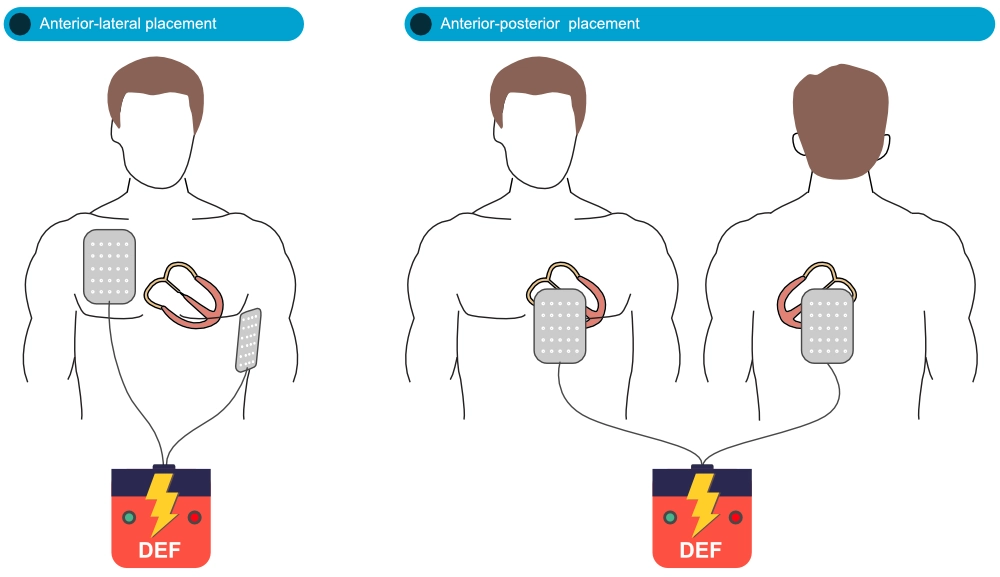
Defibrilleringselektroderne eller -padlerne skal placeres for at maksimere mængden af myokardium mellem elektroderne/padlerne (Tung et al.). Ved anterior-lateral (anterior-apikal) positioneringplaceres en elektrode/paddel til højre for brystbenet og en i venstre midtaksillærlinje (hvor EKG-afledning V6 er placeret). Ved anterior-posterior positionering, som kræver puder, placeres en pude på precordium og en på venstre nedre scapularregion (figur 5).
Moderne defibrillatorer bruger bifasiske stød til at levere den elektriske strøm. Defibrillatoren tilpasser strømmens amplitude og varighed til thorax’ impedans i henhold til producentens specifikationer. Det er afgørende at levere en tilstrækkelig stærk strøm til at afslutte arytmien. Der er i øjeblikket ingen beviser for, at noget energiniveau er optimalt, og det anbefalede energiniveau varierer afhængigt af producenten. Producentens anbefalede energiniveau til defibrillering vises altid på eller i nærheden af defibrillatorens display. Der er tre forskellige metoder til at levere en bifasisk strøm; de er aldrig blevet sammenlignet, og de er sandsynligvis lige effektive (Soar et al.).
For at minimere tiden uden strøm kan defibrillatoren oplades mod slutningen af hver kompressionscyklus (foropladning), så den er klar til at give stød med det samme, hvis rytmen er stødbar. Hvis rytmetjekket ikke viser en stødbar rytme, genoptages kompressionerne med det samme.
Nogle defibrillatorer kan filtrere (eliminere) bevægelsesartefakter og dermed vise det faktiske EKG-signal under igangværende kompressioner. Ellers er det normalt umuligt at se det underliggende EKG-signal, når kompressionerne er i gang.

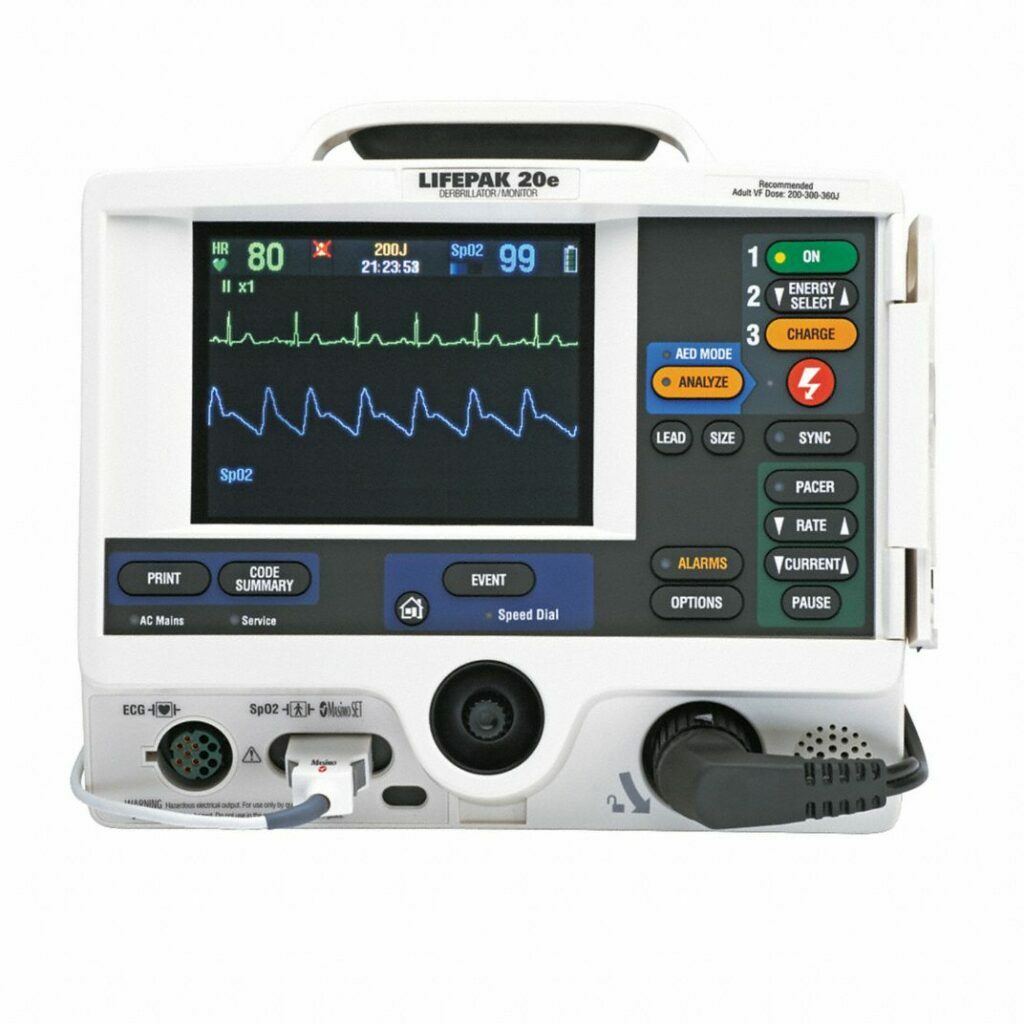

Risikoen ved at tilføre høje energiniveauer til hjertet og andet væv under hjertestop anses for at være ubetydelig. Ingen producenter designer defibrillatorer, der kan levere mere end 360 Joule, hvilket anses for at være sikkert. Dette er blevet bekræftet i undersøgelser af troponiner, EKG-ændringer og venstre ventrikels funktion efter elektrisk kardioversion med 360 J. Energiniveauer mellem 150 J og 360 J anvendes ved hjertestop. Se venligst hver enkelt producents anbefalinger.
Hvis rytmen er stødbar, forsøges én defibrillering, og kompressionerne genoptages umiddelbart efter defibrilleringen. Rytme- og pulstjek udføres efter næste cyklus. Undtagelsen fra denne regel er et overværet hjertestop med stødbar rytme og en defibrillator, der er umiddelbart tilgængelig; i disse tilfælde kan man give op til tre defibrilleringer (med puls- og rytmetjek mellem defibrilleringerne), før man starter almindelig HLR med kompressioner. Begrundelsen for dette er, at kompressioner er mindre gavnlige i løbet af de første 4 minutter efter kollapset.
Eskalering af energiniveau
Hvis en defibrillering ikke afslutter arytmien, kan den næste defibrillering give enten med et uændret eller højere energiniveau. Der er ingen undersøgelser, der viser, at optrapning af energiniveauer (leveret af en defibrillator) påvirker overlevelsen ved hjertestop. Eskalering er dog forbundet med færre defibrilleringer, hvilket tyder på en fordel. Derfor anbefales det, at energiniveauet øges, hvis defibrillering mislykkes (Soar et al.).
Refibrillering og chokrefraktær ventrikelflimmer
Ca. 50 % af alle tilfælde af OHCA med ventrikelflimmer (VF) eller pulsløs ventrikulær takykardi (VT) forbliver i VF/VT på trods af gentagne defibrilleringsforsøg (Link et al, Morrison et al, Spies et al, Holmén et al). VF/VT, der fortsætter efter 3 defibrilleringer, defineres som refraktær VF (stødrefraktær VF). Retningslinjer har anbefalet følgende i tilfælde af refraktær VF/VT:
- Kontrollér elektrodernes/padlernes position.
- Øg energiniveauet til maksimal energi (360 J).
Cheskes et al. sammenlignede tre defibrilleringsstrategier for refraktær VF:
- Standard defibrillering.
- Vector change (VC) defibrillering (dvs. anterior-lateral position skiftes til anterior-posterior).
- Dobbelt sekventiel ekstern defibrillering (DSED), som indebærer hurtig afgivelse af to sekventielle stød ved hjælp af to defibrillatorer, den ene med anterior-lateral og den anden med anterior-posterior position.
Undersøgelsen, som omfattede 404 patienter, viste, at overlevelsen til udskrivning fra hospitalet var 30,4 % i DSED-gruppen, 21,7 % i VC-gruppen og 13,3 % med standarddefibrillering. Der er behov for flere undersøgelser for at afgøre, om DSED bør være strategien ved refraktær VF/VT eller mere generelt i alle tilfælde af stødbar rytme.
Patienter med implanterbar cardioverter-defibrillator (ICD)
De fleste ICD’er implanteres under den venstre brystmuskel. En ICD defibrillerer med 40 J, hvilket er smertefuldt for bevidste patienter. Den elektriske strøm, der genereres af en ICD, udgør dog ikke nogen risiko for reddere, der rører ved kroppen.
Subkutane ICD’er implanteres i den forreste aksillærlinje under brystmusklen. Disse ICD-systemer har én ledning, som fører subkutant mod brystbenet og op langs venstre brystbensrand. Subkutane ICD’er afgiver stød med 80 J, hvilket sandsynligvis er lige så effektivt som transvenøse ICD’er (Knops et al.). Redningsfolk, der giver manuelle kompressioner, kan opleve et ubehageligt, men ufarligt stød.
Elektrisk konvertering af ventrikulær takykardi (VT)
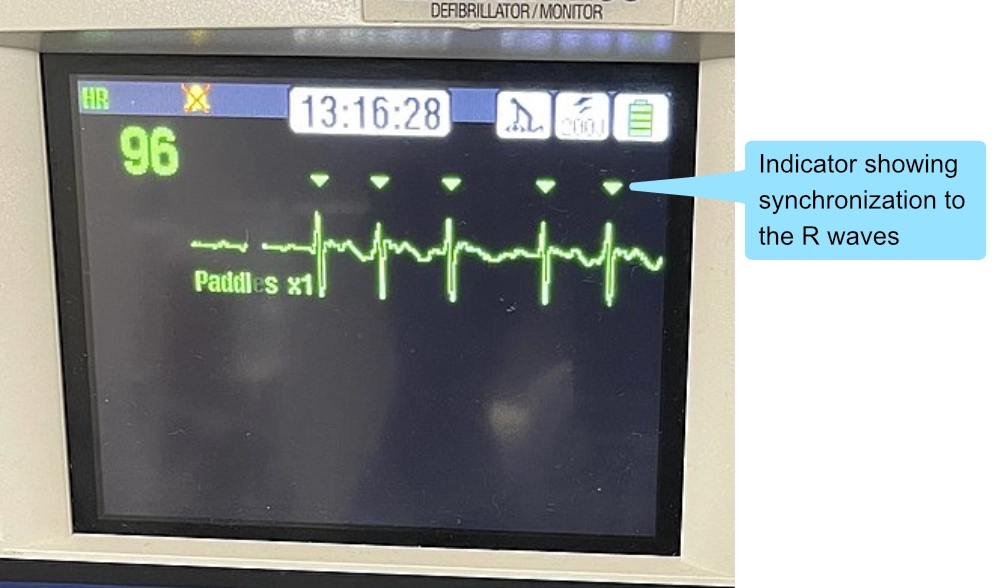
Ventrikulær takykardi kan afsluttes ved hjælp af elektrisk konvertering (dvs. synkroniseret stød), typisk med 150 J, med optrapning af energiniveauet efter behov. Stødet skal være synkroniseret, ellers er der risiko for at fremkalde ventrikelflimmer. Synkroniserede stød afgives på R-bølgen, hvilket har til hensigt at undgå at afgive elektrisk strøm under T-bølgens apex, som er en elektrisk sårbar fase i hjertets cyklus.
Alle defibrillatorer viser indikatorer på EKG-kurven, som angiver, hvor den synkroniserede strøm vil blive afgivet (figur 7). Hvis synkroniseringen er aktiveret, men indikatorerne mangler, er synkroniseringen sandsynligvis ikke aktiveret (det kan skyldes vanskeligheder med at fortolke rytmen). I sådanne scenarier er der flere muligheder: (1) Flyt EKG-afledningerne, øg spændingsforstærkningen på defibrillatoren, eller deaktiver synkroniseringen. Hvis en organiseret rytme defibrilleres med et ikke-synkroniseret stød, skal man være klar til at defibrillere (ikke-synkroniseret) ventrikelflimmer, der måtte opstå.
Defibrillering udgør ingen risiko for fostre.
Vellykket defibrillering (ROSC)
Hvis defibrillering lykkes med at afslutte en ventrikulær arytmi og etablere sinusrytme, tager det normalt et par sekunder, før de ventrikulære sammentrækninger begynder. Derfor forventes det, at pulsen ikke kan mærkes i løbet af de første sekunder af genoprettelsen af sinusrytmen (Sunde et al, Rea et al). Dette forklares med myocardial stunning, som indebærer, at myocardiet er bedøvet (en akinetisk eller alvorlig hypokinetisk) efter genoprettelse af blodgennemstrømningen efter langvarig iskæmi. Det kan tage op til 2 minutter, før de ventrikulære sammentrækninger normaliseres (Pierce et al.).
Resumé af defibrillering
- Defibriller med bifasisk strøm ved hjælp af det energiniveau (for VF), der anbefales af producenten.
- Det mindste energiniveau for VF er 150 J. Det maksimale sikre energiniveau er 360 J.
- Hvis følgende tre betingelser er opfyldt, kan der testes op til 3 defibrilleringer uden kompressioner:
- (1) Vidne til hjertestop,
- (2) indledende rytme er VF/VT og
- (3) defibrillatoren er tilsluttet eller umiddelbart tilgængelig.
- Overvej at oplade defibrillatoren mod slutningen af kompressionscyklussen, så den er klar til at defibrillere med det samme, hvis rytmen er stødbar. Hvis defibrillatoren ikke er opladet, skal kompressionerne fortsætte, indtil den er klar til at affyre.
- Efter en defibrillering fortsætter kompressionerne med det samme (i 2 minutter). Rytme- og pulstjek udføres ved næste tjek.
- Defibrillering kan udføres under igangværende mekaniske kompressioner.
Takyarytmi med forestående hjertestop
Hvis en bevidst person med takyarytmi udviser tegn på cirkulatorisk ustabilitet, skal der straks udføres elektrisk kardioversion for at forhindre udvikling til hjertestop.
Kardioversion er smertefuldt hos bevidste patienter, hvilket kan håndteres ved hjælp af sedativer (midazolam) eller analgetika (morfin):
- Midazolam: 1-3 mg startdosis. Samlet dosis 4-8 mg. Lavere dosis i tilfælde af alder > 60 år.
- Morfin: 2,5 mg IV.
Typen af takyarytmi – supraventrikulær eller ventrikulær – er irrelevant for beslutningen om at udføre kardioversion. Ved atrieflimren bør elektrisk kardioversion anvende det maksimale energiniveau (360 J), hvis patienten er ustabil (selvom 200 J er tilstrækkeligt i de fleste tilfælde). Andre typer af atrial takyarytmi – herunder atrieflagren, atrial takykardi og multifokal atrial takykardi – kræver typisk lavere energiniveauer (70 J til 120 J). Hvis elektrisk kardioversion mislykkes, og patienten forbliver hæmodynamisk stabil, kan der gøres et nyt forsøg sammen med en intravenøs infusion af 300 mg amiodaron over 10-20 minutter. Dette vil øge sandsynligheden for en vellykket kardioversion. Procainamid er et rimeligt alternativ (10-15 mg/kg over 20 minutter).
Ved hæmodynamisk stabile ventrikulære arytmier kan farmakologisk behandling forsøges først. Atrieflimren kan også kontrolleres ved hjælp af amiodaron, betablokkere eller digoxin. Amiodaron er sikkert hos patienter med svær dysfunktion i venstre ventrikel.
Midlertidig pacing ved hjertestop
Moderne defibrillatorer kan udstyres med en pacemakerfunktion. Denne funktion bruges til transkutan pacing. Pacemakeren bør testes i alle situationer, hvor der er grund til at tro, at transkutan stimulering kan fremkalde elektrisk og mekanisk indfangning (dvs. fremkalde ventrikulære sammentrækninger). Farmakologisk behandling af bradykardi er beskrevet i kapitlet Behandling af bradykardi.
Transkutan pacemaker
Evidens: Klasse I anbefaling
- En pacemaker er den sikreste behandling af akut bradykardi.
- En transkutan pacemaker bør etableres med det samme, hvis der er risiko for hæmodynamisk kollaps.
- AV-blok 2 Mobitz type 2 og AV-blok 3 er stærke indikationer for transkutan pacemaker.
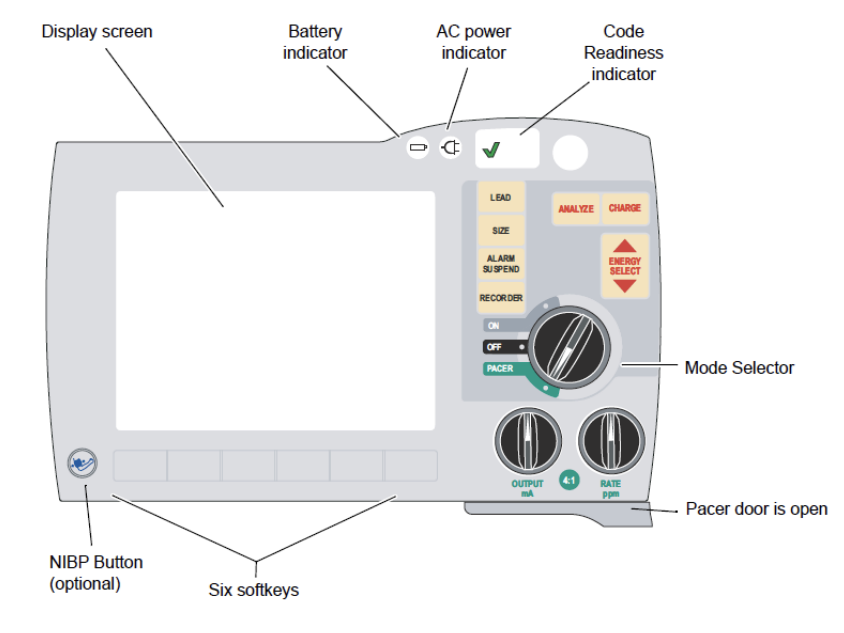
Sådan udføres transkutan pacing
- Forklar patienten formålet med proceduren.
- Giv beroligende/analgetisk medicin:
- Midazolam: 1-3 mg startdosis. Samlet dosis 4-8 mg. Lavere dosis i tilfælde af alder > 60 år.
- Morfin: 2,5 mg IV.
- Placer elektroderne i anterior-posterior retning.
- Hvis der er tid, trimmes bryst- og ryghår (må ikke barberes). Tør huden, hvis den er våd.
- Flyt ikke allerede fastgjorte elektroder (klæberen bliver dårlig).
- Aktivér pacemakerfunktionen.
- Indstil pacingfrekvensen til 50 slag/min.
- Øg gradvist strømmen (start med 20 mA).
- Identificer pacemakerens spikes (stimuleringsartefakter) på EKG-optagelsen.
- Find ud af, om pacemakerpiggene efterfølges af QRS-komplekser (hvilket indikerer elektrisk indfangning).
- Hvis elektrisk indfangning er synlig, skal du palpere arteria femoralis for at undersøge, om der er mekanisk indfangning (dvs. ventrikulære sammentrækninger).
- Overvåg blodtryk og pulsoxymetri.
- Når tærsklen for indfangning (laveste strøm, der giver mekanisk indfangning) er identificeret, øges output (strøm) med 10 % (for at give stimuleringer med en sikkerhedsmargin).
- De fleste patienter har brug for en strøm i området 20 til 140 mA
- Undgå unødvendig pacing ved at bruge en lav basisfrekvens (f.eks. 30-40 slag/min).
Sådan udføres transkutan pacing under asystoli
Følg samme procedure som ovenfor, men start med maksimal strømstyrke (output), og reducer gradvist strømmen, indtil stimuleringen ikke giver capture. Derefter øges strømmen, indtil der opnås capture, og yderligere 10 % output som sikkerhedsmargin.
Kontrol af transkutan pacing
- Mekanisk capture bekræftes ved at palpere en perifer puls (arteria femoralis) eller vurdere pulsoximetri. Undgå at vurdere pulsen i halspulsåren (sammentrækninger i brystmusklerne kan forveksles med arterielle pulseringer).
- Muskelsammentrækninger svarer ikke til mekanisk indfangning.
- Hvis pacemakeren stimulerer mere end nødvendigt, er der undersensing, hvilket betyder, at pacemakeren ikke registrerer de ventrikulære komplekser (og derfor fortsætter med at pace). Dette løses ved at flytte EKG-afledningerne, så de registrerer større QRS-amplituder, eller ved at øge forstærkningen på defibrillatoren.
- Hvis pacemakeren ikke stimulerer på grund af artefakter, er der tale om oversensing, som kan løses ved at fjerne artefakterne eller flytte afledningerne.
Lægemidler ved hjertestop
Intravenøs adgang
Forsøg at etablere intravenøs (iv) adgang. Hvis der ikke kan etableres intravenøs adgang, skal der etableres intraossøs (io) adgang.
Adrenalin (epinephrin) ved hjertestop
Dosis og indikationer
- Adrenalin 1 mg giver straks, hvis den første rytme ikke er stødbar (asystoli, PEA).
- Adrenalin 1 mg giver efter den tredje defibrillering ved stødbar rytme.
- Adrenalin 1 mg giver hvert fjerde minut under HLR.
Adrenalin er en vasopressor med inotrope og kronotrope virkninger. Adrenalin kan opnå følgende under et hjertestop:
- Adrenalin øger det koronare perfusionstryk (CPP).
- Adrenalin kan fremkalde elektrisk aktivitet i myokardiet
- Adrenalin kan omdanne fin ventrikelflimmer (som er mindre egnet til defibrillering) til grov ventrikelflimmer (som er mere egnet til defibrillering).
- Adrenalin øger hjertefrekvensen ved bradykardi.
- Adrenalin kan forbedre den elektriske stabilitet.
- Adrenalin kan fremkalde mekanisk kobling ved PEA.
- Adrenalin øger kontraktiliteten (inotrop effekt).
- Adrenalin hæver blodtrykket.
- Adrenalin øger sandsynligheden for at lykkes med defibrillering.
- Højere doser af adrenalin (5 mg vs. 1 mg) resulterer i en højere frekvens af ROSC, men påvirker ikke overlevelsen (Lin et al.). Desuden forårsagede højere doser adrenalin dårligere myokardiefunktion hos patienter, der blev behandlet på intensivafdelingen. Høje doser af adrenalin frarådes.
På intensivafdelingen kan adrenalin erstattes med dopamin eller dobutamin, hvis der ønskes en inotrop effekt uden kronotrop effekt.
I den største randomiserede kontrollerede undersøgelse af adrenalin ved hjertestop uden for hospital (PARAMEDIC 2) blev der draget følgende konklusioner (Perkins et al):
- Adrenalin resulterede i en 39 % højere sandsynlighed for overlevelse efter 30 dage (forskellen var statistisk signifikant, og det var undersøgelsens primære resultat).
- Adrenalin resulterede i 18 % større sandsynlighed for at blive udskrevet i live, men denne forskel var ikke statistisk signifikant.
- I adrenalin-gruppen var det neurologiske resultat dårligere.
Samlet set øger adrenalinoverlevelsen efter 30 dage på bekostning af neurologiske skader, som er mere alvorlige og hyppigere i adrenalingruppen. Det kan forklares med binyrebarkens negative indvirkning på den cerebrale mikrovaskulære blodgennemstrømning (Ristagno et al, Deakin et al).
Antiarytmiske lægemidler: amiodaron og lidocain
- Antiarytmika administreres, hvis en ventrikulær arytmi (VF, VT) ikke kan afsluttes med defibrillering.
- Amiodaron 300 mg giver til voksne med VF/VT efter den tredje defibrillering.
- Amiodaron 150 mg giver til voksne med VF/VT efter den femte defibrillering.
- Lidocain 100 mg giver, hvis amiodaron ikke er tilgængeligt, eller hvis arytmien er torsade de pointes (TDP). Der kan gives yderligere 50 mg lidokain efter den femte defibrillering.
- Ved akut (transmural) myokardieinfarkt er lidokain sandsynligvis mere effektivt end amiodaron.
- I tilfælde af ROSC og fortsatte ventrikulære arytmier kan amiodaron gives som en kontinuerlig infusion til en samlet daglig dosis på 1200 mg.
I en sammenligning mellem amiodaron, lidokain og placebo er overlevelsen ved udskrivelsen den samme, men placebo får en lavere andel til at blive indlagt i live ved OHCA. Både amiodaron og lidokain resulterer i højere overlevelsesrater, når der ydes HLR af tilskuere. Effekten af disse lægemidler er usikker ved intraossøs administration (Kudenchuk et al, Daya et al).
Amiodaron udgør ingen risiko for fostre.
Betablokkere
Betablokkere (metoprolol, esmolol) og magnesium bør overvejes i følgende situationer:
- polymorf VT, der ikke reagerer på amiodaron.
- Torsade de pointes (TDP)
- Monomorf hurtig VT eller ventrikelflagren.
- Refraktær VF eller VT.
Magnesium (magnesiumsulfat)
Magnesiumsulfat 2 g iv giver altid ved torsade de pointes (uanset magnesiumniveauet i blodet). Injektionen kan gentages og bruges som infusion.
Calcium (calciumgluconat)
10 ml 10% calciumgluconat indsprøjtes ved svær hyperkaliæmi, hypocalcæmi eller overdosering af calciumkanalblokkere.
Natriumbikarbonat
Natriumbikarbonat kan give ved hyperkaliæmi og overdosis af lægemidler (forgiftning).
Væske
Væske skal gives hurtigt, hvis der er mistanke om hypovolæmisk hjertestop.
Trombolyse
Hvis lungeemboli er den underliggende årsag til hjertestoppet, skal der gives trombolyse:
- Alteplase (Activase®, Actilyse®): Alteplase opbevares i ampuller. Ampullerne I og II blandes i henhold til anvisningerne på pakken til en koncentration på 1 mg/ml. Giv en bolus på 0,6 mg/kg (maks. 50 mg) i.v. og derefter en infusion på 50 mg over 90 minutter (samlet dosis maks. 1,5 mg/kg ved kropsvægt <65 kg).
Tegn på ROSC
Tegnene på ROSC ved hjertestop er som følger:
- Bevægelser
- Målbart blodtryk
- Kraftig stigning i ETCO2
- Opvågning
HLR sættes på pause for at kontrollere hjertefrekvens og rytme, hvis disse tegn opstår.
Referencer
Tung L, Sliz N, Mulligan MR. Indflydelse af elektrisk stimuleringsakse på excitation af hjertemuskelceller.Circ Res. 1991; 69:722-730. doi: 10.1161/01.res.69.3.722
Steen S, Liao Q, Pierre L, Paskevicius A, Sjoberg T. Den kritiske betydning af minimal forsinkelse mellem brystkompressioner og efterfølgende defibrillering: en hæmodynamisk forklaring. Resuscitation. 2003; 58: 249-258.
Tang W, Snyder D, Wang J, Huang L, Chang YT, Sun S, Weil MH. En defibrilleringsprotokol med ét stød versus tre stød forbedrer udfaldet betydeligt i en svinemodel af langvarig ventrikelflimmer-hjertestop. Circulation. 2006; 113: 2683-2689.
Redberg. Sham Controls in Medical Device Trials Liste over forfattere. N Engl J Med 2014; 371:892-893 DOI: 10.1056/NEJMp1406388
Talikowska M, Tohira H, Finn J. Kvaliteten af hjertelungeredning og patientens overlevelse ved hjertestop: En systematisk gennemgang og metaanalyse. Resuscitation. 2015;96:66-77. doi: 10.1016/j. resuscitation.2015.07.036
Christenson J, Andrusiek D, Everson-Stewart S, Kudenchuk P, Hostler D, Powell J, Callaway CW, Bishop D, Vaillancourt C, Davis D, Aufderheide TP, Idris A, Stouffer JA, Stiell I, Berg R; Resuscitation Outcomes Consortium Investigators. Brystkompressionsfraktion bestemmer overlevelse hos patienter med ventrikelflimmer uden for hospital. Circulation. 2009;120:12411247. doi: 10.1161/CIRCULATIONAHA.109.852202
Vaillancourt C, Everson-Stewart S, Christenson J, Andrusiek D, Powell J, Nichol G, Cheskes S, Aufderheide TP, Berg R, Stiell IG; Resuscitation Outcomes Consortium Investigators. Virkningen af øget brystkompressionsfraktion på tilbagevenden af spontan cirkulation for hjertestoppatienter uden for hospitalet, der ikke er i ventrikelflimmer. Genoplivning. 2011;82:1501-1507. doi: 10.1016/j.resuscitation.2011.07.011
Sugerman NT, Edelson DP, Leary M, Weidman EK, Herzberg DL, Vanden Hoek TL, Becker LB, Abella BS. Træthed hos redningsmandskabet under faktisk hjerte-lunge-redning på hospitalet med audiovisuel feedback: et prospektivt multicenterstudie. Resuscitation. 2009;80:981-984. doi: 10.1016/j.resuscitation.2009.06.002
Mechanical Chest Compressions and Simultaneous Defibrillation vs Conventional Cardiopulmonary Resuscitation in Out-of-Hospital Cardiac Arrest The LINC Randomized Trial Sten Rubertsson, MD, PhD1; Erik Lindgren, MD1; David Smekal, MD, PhD1; et alOllie Östlund, PhD2; Johan Silfverstolpe, MD3; Robert A. Lichtveld, MD, PhD4; Rene Boomars, MPA4; Björn Ahlstedt, MD5; Gunnar Skoog, MD6; Robert Kastberg, MD6; David Halliwell, RN7; Martyn Box, RN7; Johan Herlitz, MD, PhD8; Rolf Karlsten, MD, PhD1 Author Affiliations Article Information JAMA. 2014;311 (1):53-61. doi:10.1001/jama.2013.282538
Brug af backboards i hjerte-lunge-redning: en systematisk gennemgang og metaanalyse Matteo Paganini 1, Giulia Mormando 2, Fabio Carfagna 3, Pier Luigi Ingrassia 3 Affiliations expand PMID: 33417354 DOI: 10.1097/MEJ.0000000000000784
Guildner CW. Genoplivning – åbning af luftvejene: en sammenlignende undersøgelse af teknikker til åbning af luftveje, der er blokeret af tungen. JACEP. 1976;5:588-590. doi: 10.1016/s0361-1124 (76)80217-1
Lin S, Callaway CW, Shah PS, et al. Adrenalin til genoplivning af hjertestop uden for hospital: en systematisk gennemgang og metaanalyse af randomiserede kontrollerede forsøg. Resuscitation 2014;85:732-740.
Retningslinjer 2000 for hjerte-lunge-redning og akut kardiovaskulær behandling. 6. Avanceret kardiovaskulær livsstøtte: afsnit 6: farmakologi II: midler til optimering af hjertets output og blodtryk. Circulation 2000;102:Suppl:I-129–I-135.
Link MS, Atkins DL, Passman RS, et al. Electrical therapies: automated external defibrillators, defibrillation, cardioversion, and pacing: 2010 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care. Cirkulation 2010;122:Suppl 3:S706-S719.
Kudenchuk PJ, Brown SP, Daya M, et al. Amiodarone, lidocaine, or placebo in out-of-hospital cardiac arrest. N Engl J Med 2016;374:1711-1722.
Morrison LJ, Dorian P, Long J, et al. Out-of-hospital cardiac arrest rectilinear biphasic to monophasic damped sinus defibrillation waveforms with advanced life support intervention trial (ORBIT). Resuscitation 2005;66:149-157.
Spies DM, Kiekenap J, Rupp D, Betz S, Kill C, Sassen MC. Tid til at ændre tiderne? Tidspunkt for gentagelse af ventrikelflimmer under OHCA. Resuscitation 2020;157:219-224.
Holmén J, Hollenberg J, Claesson A, et al. Overlevelse ved ventrikelflimmer med vægt på antallet af defibrilleringer i forhold til andre faktorer ved genoplivning. Genoplivning 2017;113:33-38.
Aufderheide TP, Sigurdsson G, Pirrallo RG, Yannopoulos D, McKnite S, von Briesen C, Sparks CW, Conrad CJ, Provo TA, Lurie KG. Hyperventilationsinduceret hypotension under kardiopulmonal genoplivning. Circulation. 2004;109:1960-1965. doi: 10.1161/01.CIR.0000126594.79136.61
Hypotermi versus normotermi efter hjertestop uden for hospital Liste over forfattere. Josef Dankiewicz, M.D., Ph.D., Tobias Cronberg, M.D., Ph.D., Gisela Lilja, O.T., Ph.D., Janus C. Jakobsen, M.D., Ph.D., Helena Levin, M.Sc., Susann Ullén, Ph.D., Christian Rylander, M.D., Ph.d., Matt P. Wise, M.B., B.Ch., D.Phil., Mauro Oddo, M.D., Alain Cariou, M.D., Ph.D., Jan Bělohlávek, M.D., Ph.D., Jan Hovdenes, M.D., Ph.D., et al. for TTM2 Trial Investigators. N Engl J Med 2021; 384:2283-2294 DOI: 10.1056/NEJMoa2100591
Jabre P, Penaloza A, Pinero D, Duchateau FX, Borron SW, Javaudin F, Richard O, de Longueville D, Bouilleau G, Devaud ML, Heidet M, Lejeune C, Fauroux S, Greingor JL, Manara A, Hubert JC, Guihard B, Vermylen O, Lievens P, Auffret Y, Maisondieu C, Huet S, Claessens B, Lapostolle F, Javaud N, Reuter PG, Baker E, Vicaut E, Adnet F. Effekten af pose-maske-ventilation vs. endotrakeal intubation under hjerte-lunge-redning på det neurologiske resultat efter kardiorespiratorisk anfald uden for hospital: Et randomiseret klinisk forsøg. JAMA. 2018;319:779-787. doi: 10.1001/jama.2018.0156
Kleinman ME, Goldberger ZD, Rea T, Swor RA, Bobrow BJ, Brennan EE, Terry M, Hemphill R, Gazmuri RJ, Hazinski MF, Travers AH. 2017 American Heart Association Focused Update on Adult Basic Life Support and Cardiopulmonary Resuscitation Quality: En opdatering af American Heart Associations retningslinjer for hjerte-lunge-redning og akut kardiovaskulær behandling. Circulation. 2018;137:e7-e13. doi: 10.1161/CIR.0000000000000539
Tidlig ekstrakorporal HLR til refraktær hjertestop uden for hospital Liste over forfattere. Martje M. Suverein, M.D., Thijs S.R. Delnoij, M.D., Roberto Lorusso, M.D., Ph.D., George J. Brandon Bravo Bruinsma, M.D., Ph.D., Luuk Otterspoor, M.D., Ph.D., Carlos V. Elzo Kraemer, M.D., Alexander P.J. Vlaar, M.D., Ph.D., Joris J. van der Heijden, M.D., Erik Scholten, M.D., Corstiaan den Uil, M.D., Ph.D., Tim Jansen, M.D., Ph.D., Bas van den Bogaard, M.D., Ph.D., Marijn Kuijpers, M.D., Ka Yan Lam, M.D., José M. Montero Cabezas, M.D., Antoine H.G. Driessen, M.D., Ph.D., Saskia Z.H. Rittersma, M.D., Ph.D., Bram G. Heijnen, M.D., Dinis Dos Reis Miranda, M.D., Ph.d., Gabe Bleeker, M.D., Ph.d., Jesse de Metz, M.D., Ph.d., Renicus S. Hermanides, M.D., Ph.d., Jorge Lopez Matta, M.D., Susanne Eberl, M.D., Dirk W. Donker, M.D., Ph.D., Robert J. van Thiel, M.D., Sakir Akin, M.D., Ph.D., Oene van Meer, M.D., José Henriques, M.D., Ph.D., Karen C. Bokhoven, M.D., Loes Mandigers, M.D., Jeroen J.H. Bunge, M.D., Martine E. Bol, M.Sc., Bjorn Winkens, Ph.D., Brigitte Essers, Ph.D., Patrick W. Weerwind, Ph.D., Jos G. Maessen, M.D., Ph.D., and Marcel C.G. van de Poll, M.D., Ph.D. January 26, 2023 N Engl J Med 2023; 388:299-309. N Engl J Med 2023; 388:299-309 DOI: 10.1056/NEJMoa2204511
