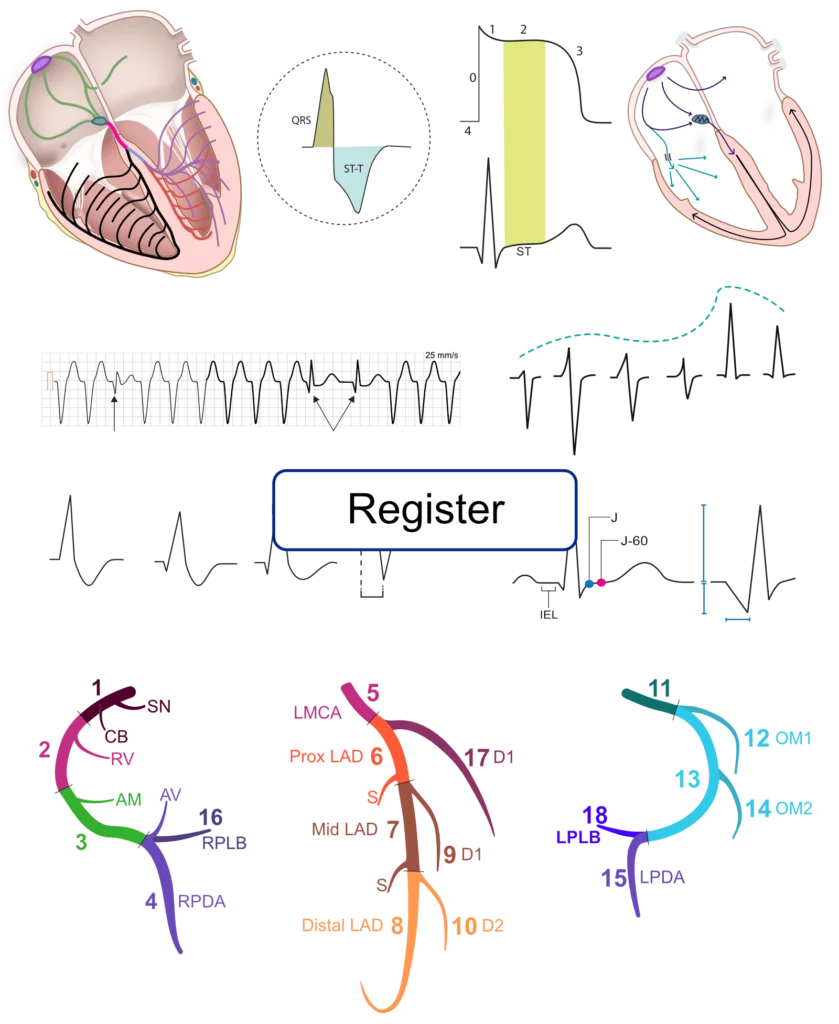
Atrieflimren: EKG, klassifikation, årsager, risikofaktorer og behandling
Atrieflimren: definitioner, årsager, risikofaktorer, EKG-diagnose og behandling
Atrieflimren er den mest almindelige abnorme takyarytmi (kun sinustakykardi er mere almindelig). Forekomsten af atrieflimren korrelerer stærkt med alderen. Omkring 10 % af personer på 80 år og derover har atrieflimren, mens arytmien er usædvanlig blandt personer under 50 år. Den samlede prævalens i en vestlig befolkning er 1,0 % til 1,5 %. Den rå prævalens er lavere i ikke-vestlige lande, primært på grund af den yngre alderssammensætning i disse lande (bloterede prævalenstal er sjældne). Den stærkeste risikofaktor for at udvikle atrieflimren er faktisk alder. Andre væsentlige risikofaktorer er følgende: mandligt køn, forhøjet blodtryk, venstre ventrikelhypertrofi, venstre ventrikeldysfunktion, hjerteklapsygdom, koronararteriesygdom, kardiomyopati, kongestivt hjertesvigt, medfødt hjertesygdom, diabetes mellitus (både type 1 og type 2), fedme, rygning, obstruktiv søvnapnø og kronisk obstruktiv lungesygdom (KOL). Desuden prædisponerer visse andre takyarytmier for at udvikle atrieflimren: atrieflagren, AVNRT og AVRT (præeksitation, WPW-syndrom) er de mest almindelige.
Atrieflimren med debut under hyperthyreoidisme (thyrotoksikose), alkoholoverdosis, thoraxkirurgi, akut myokardieinfarkt, perikarditis/myokarditis eller lungeemboli er ofte en reversibel arytmi med lav risiko for tilbagefald. Atrieflimren under andre omstændigheder (især dem, der er nævnt ovenfor) er normalt en progressiv sygdom.
Komplikationer ved atrieflimren og tilgængelige behandlinger
I multivariable modeller (dvs. statistiske modeller, hvor der kun er tale om konfunderende faktorer) har personer med atrieflimren fem gange øget risiko for slagtilfælde og to gange øget dødelighed sammenlignet med personer uden atrieflimren. Den øgede risiko for slagtilfælde forklares med dannelse af blodpropper i venstre forkammervedhæng. Sådanne blodpropper kan forlade vedhænget og komme ind i det systemiske kredsløb, hvilket forårsager tromboemboliske okklusioner af arterier i hjernen, lemmerne eller andre organer. Den øgede risiko for dødelighed kan dog ikke helt forklares med den øgede risiko for slagtilfælde; personer med atrieflimren har en øget risiko for kardiovaskulær dødelighed i almindelighed. Det er ikke overraskende i betragtning af de negative virkninger af lange perioder med takykardi og desynkroniseret atrial og ventrikulær aktivitet.
Heldigvis er behandlingen af atrieflimren kommet langt. Behandling med antikoagulation er meget effektiv til at reducere risikoen for slagtilfælde. Wrfarin og nye orale antikoagulantia kan reducere risikoen for slagtilfælde med 70 % sammenlignet med placebo. Ud over antikoagulation behandles atrieflimren med frekvens- og/eller rytmekontrol. Hastighedskontrol indebærer brug af medicin, der sænker ventrikelfrekvensen (betablokkere er grundpillen i denne behandling). Hastighedskontrol påvirker ikke rytmen i sig selv. Ved rytmekontrol forsøger man derimod at genoprette sinusrytmen ved hjælp af antiarytmika. Randomiserede, kontrollerede forsøg har ikke vist nogen klar forskel i dødelighed, når man sammenligner frekvens- og rytmekontrol. Men rytmekontrol indebærer risici (de fleste antiarytmiske lægemidler har også en proarytmisk effekt), og derfor vælger klinikere for det meste rytmekontrol. Både frekvens- og rytmekontrol reducerer morbiditet og mortalitet og forbedrer livskvaliteten. Disse tilgange diskuterer yderligere nedenfor.
Symptomer på atrieflimren
Omkring 25 % af alle personer med atrieflimren er asymptomatiske (de har ingen symptomer). Hos disse personer kan screening med EKG afsløre atrieflimren. Desværre opdages atrieflimren alt for ofte først ved hospitalsindlæggelse på grund af dens komplikationer (slagtilfælde, tromboembolisme, hjertesvigt, dyspnø). De fleste personer oplever dog symptomer, og de gør det, før de udvikler komplikationer. Symptomer som hjertebanken, dyspnø, træthed, ubehag i bryst/hals og nedsat træningskapacitet er almindelige og kan alle forekomme samtidig. Svimmelhed er også almindeligt. Synkope er dog ualmindeligt. Hvis en patient med atrieflimren oplever episoder med synkope eller endda præ-synkope, skal man mistænke tachy-brady-syndrom, hvilket indebærer, at der er en samtidig sinusknudedysfunktion. Atrieflimren, der debuterer med kongestiv hjerteinsufficiens, er ualmindelig blandt personer med tidligere normal venstre ventrikelfunktion.
Bemærk, at takyarytmi-symptomerne ved atrieflimren (hjertebanken, ubehag i brystet osv.) opstår pludseligt, og patienterne rapporterer typisk, at hjertebanken startede pludseligt.
EKG ved atrieflimren
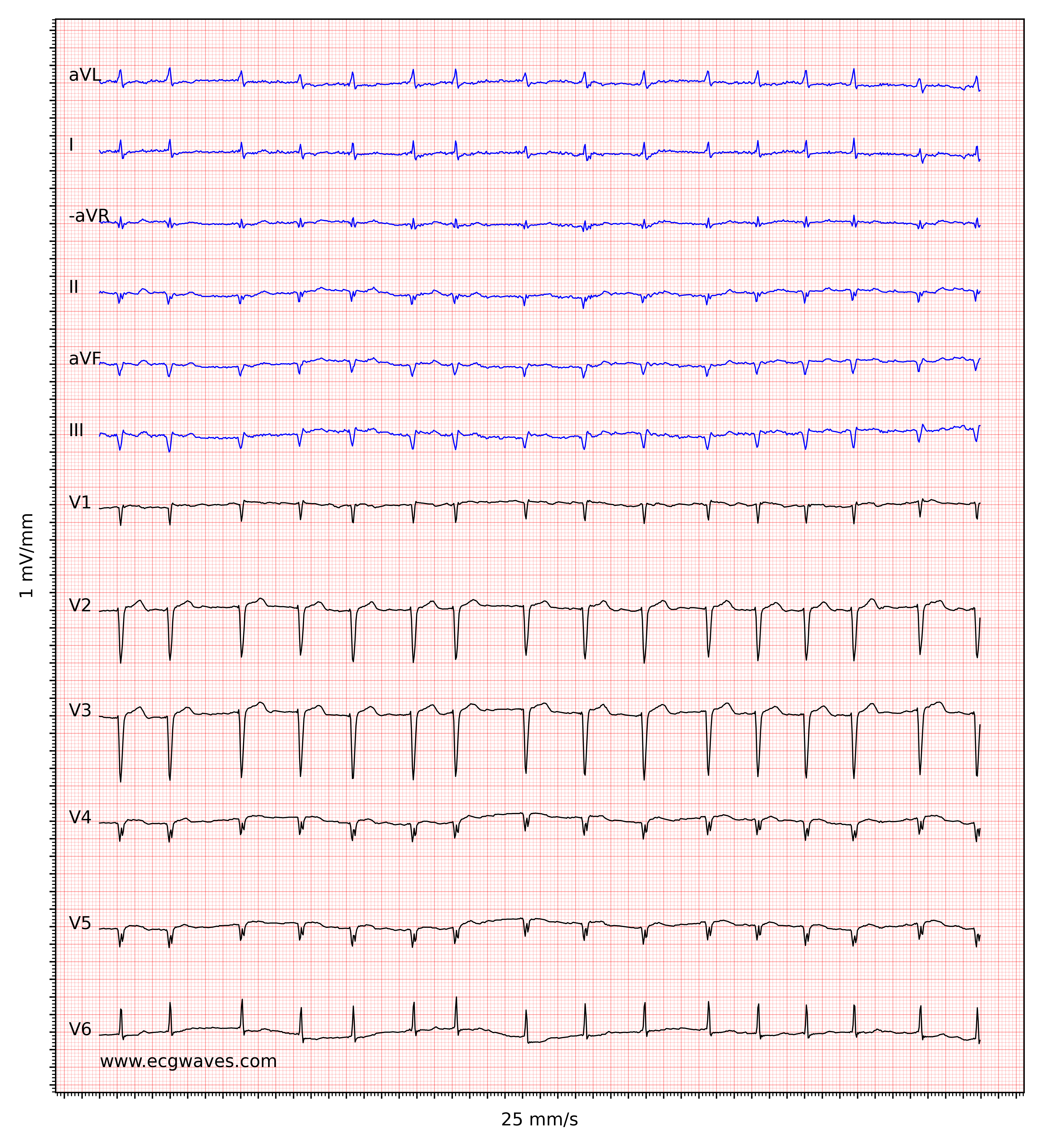
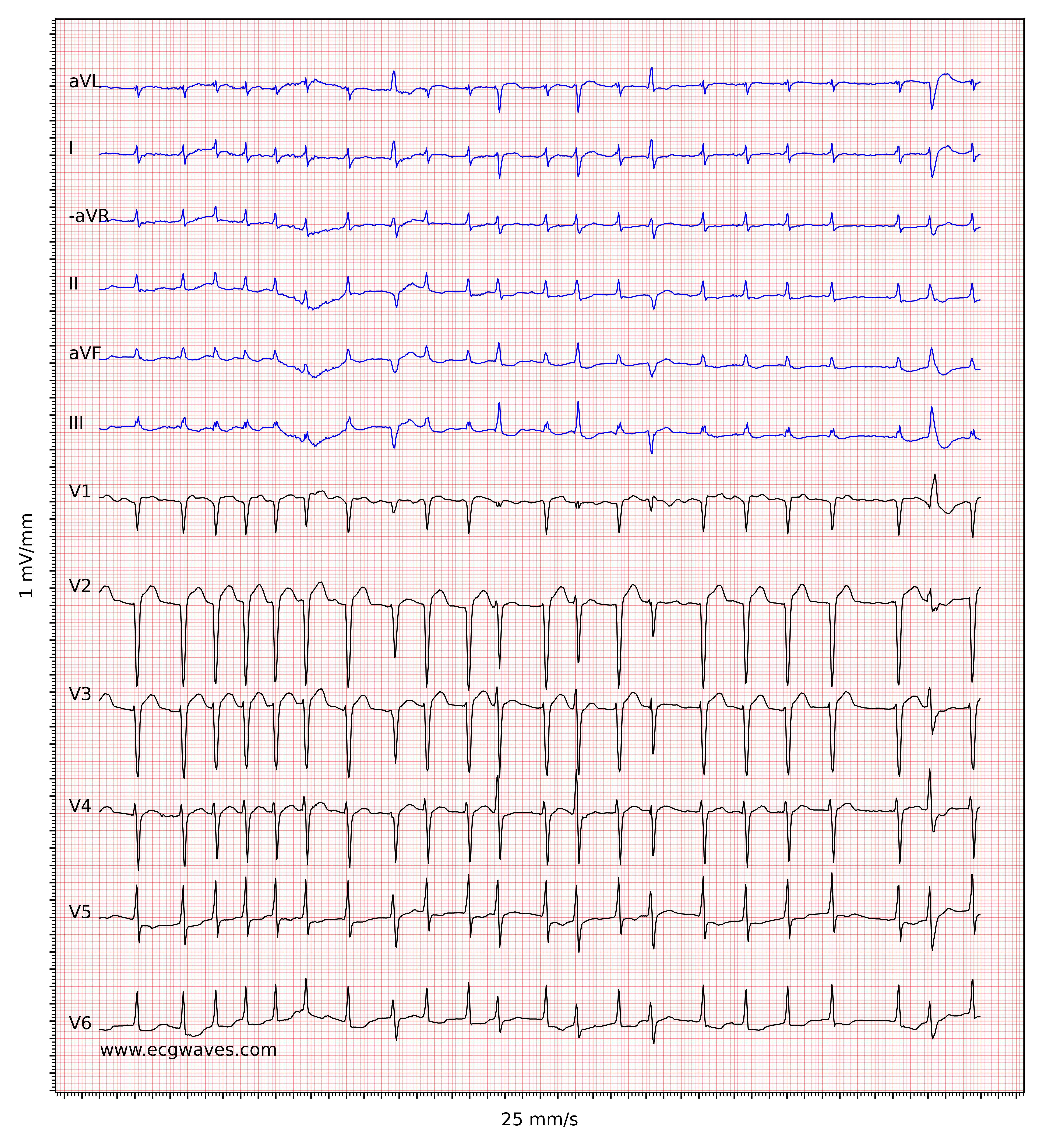
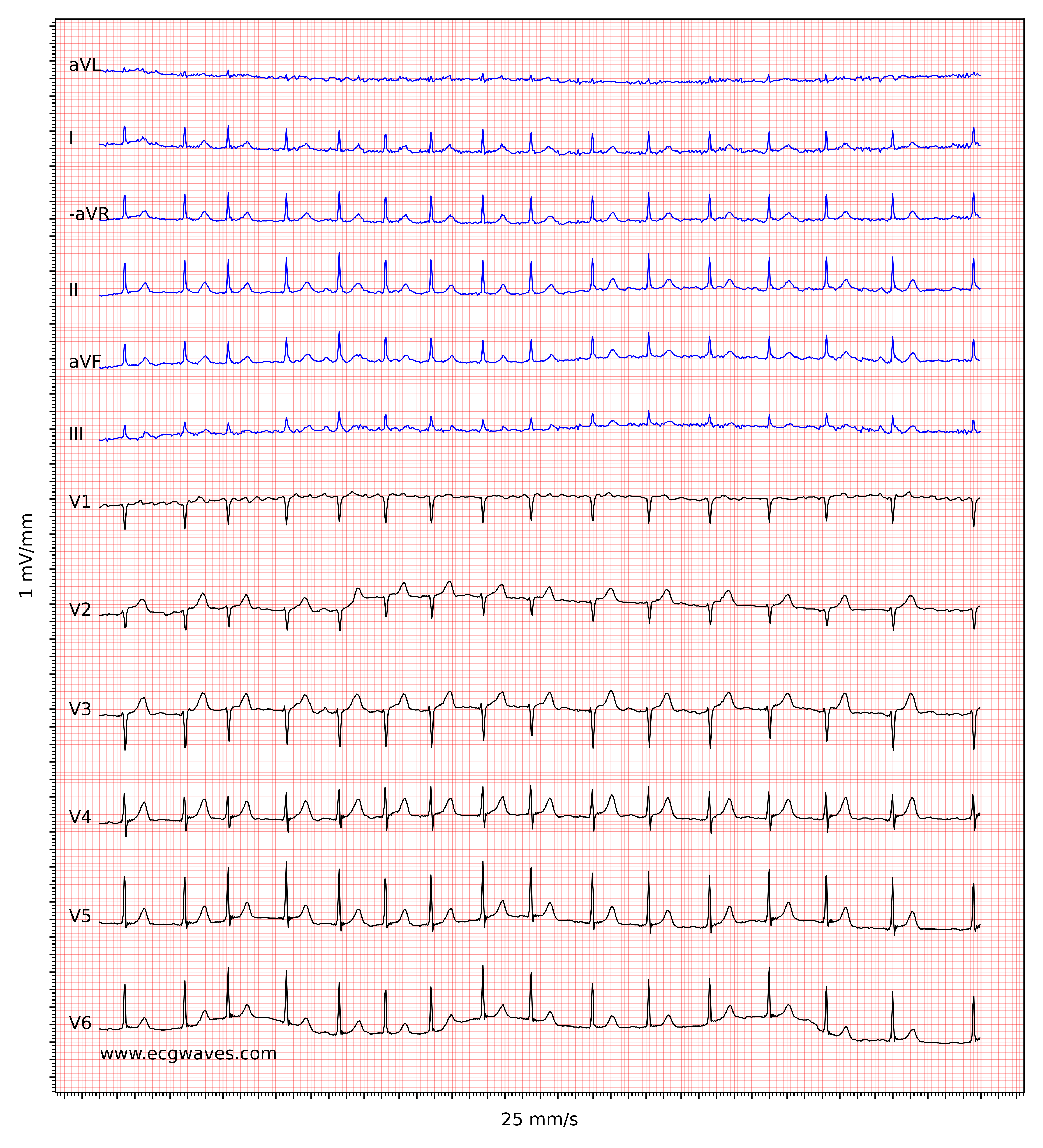
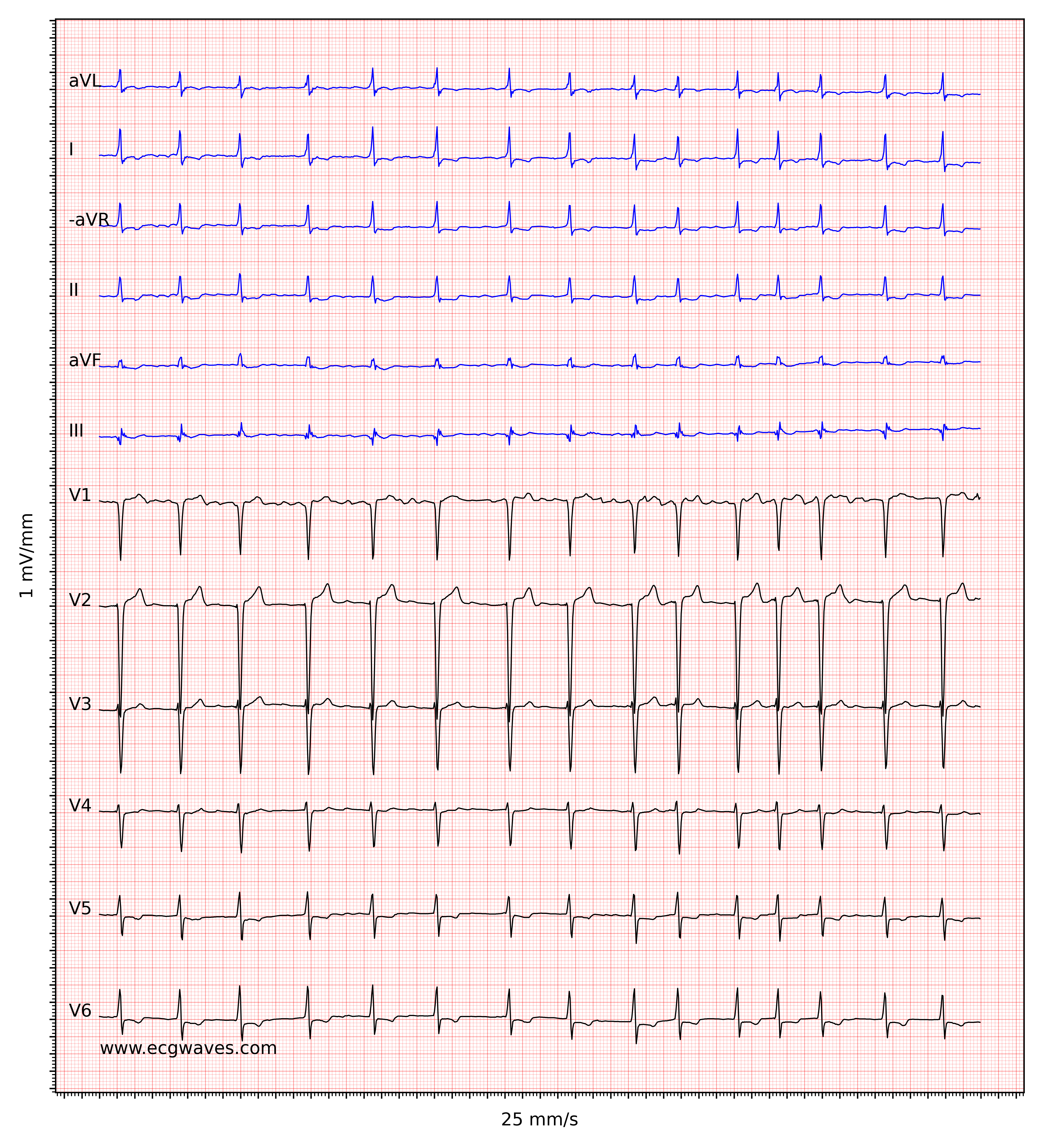
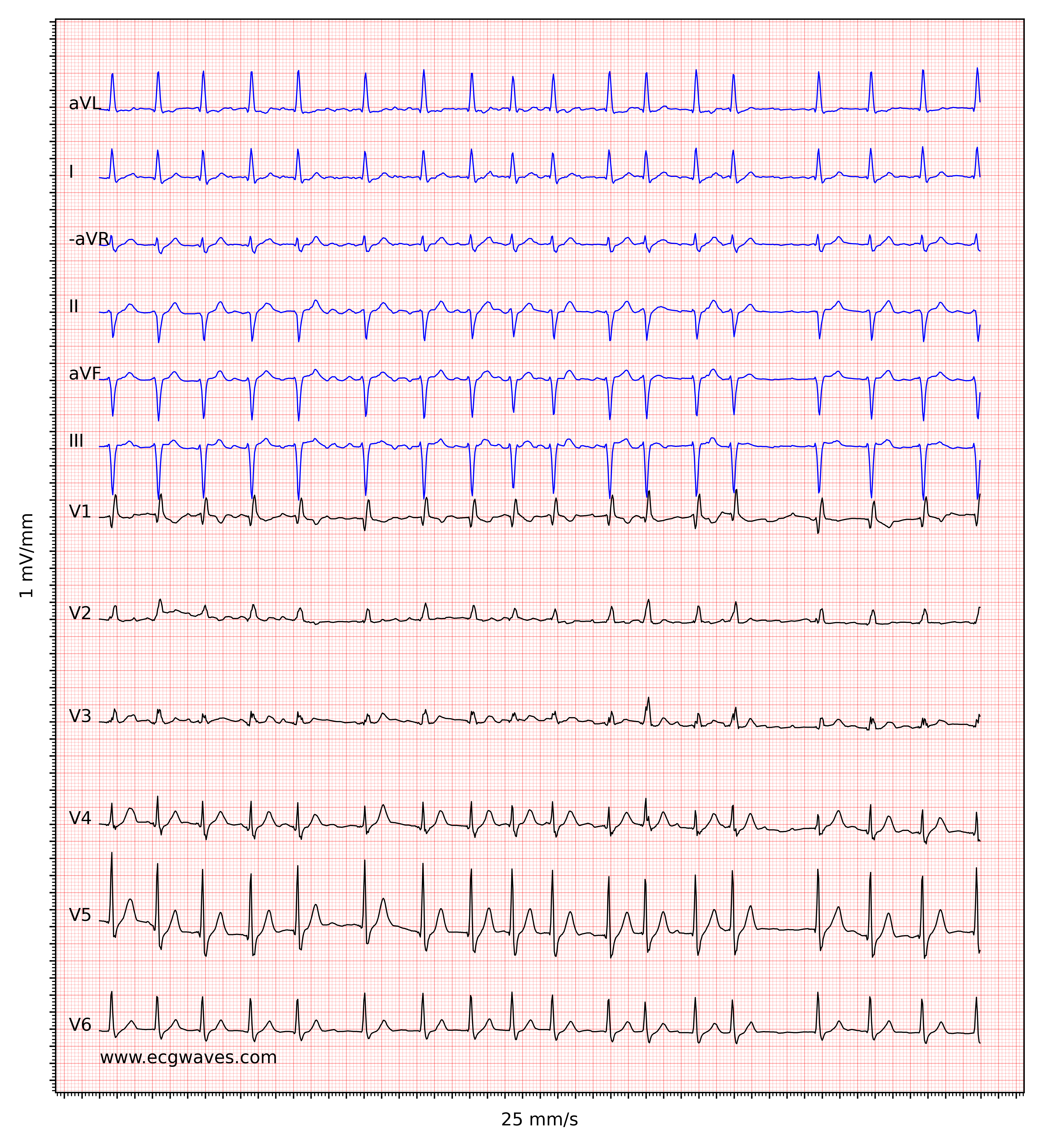
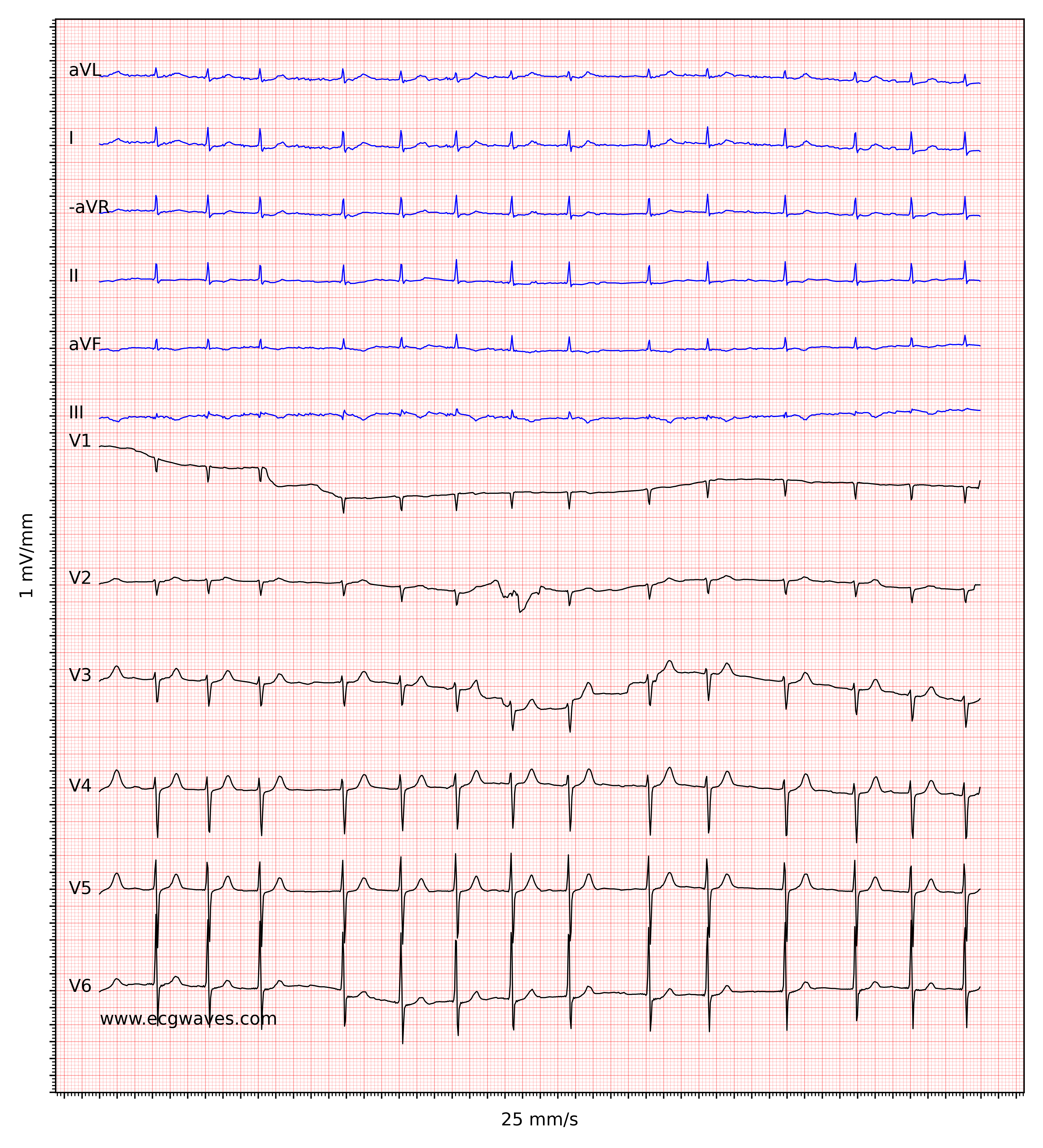
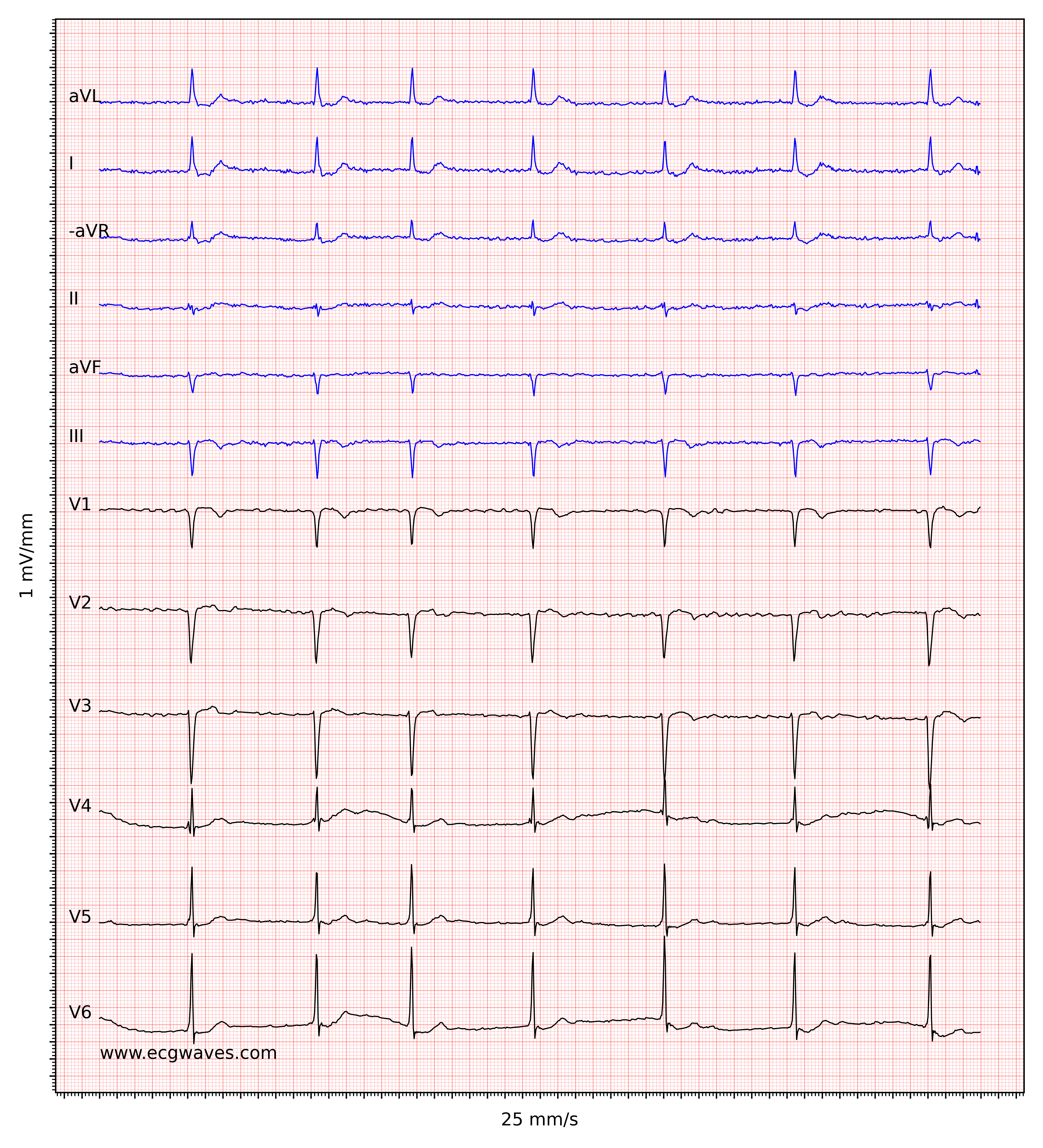
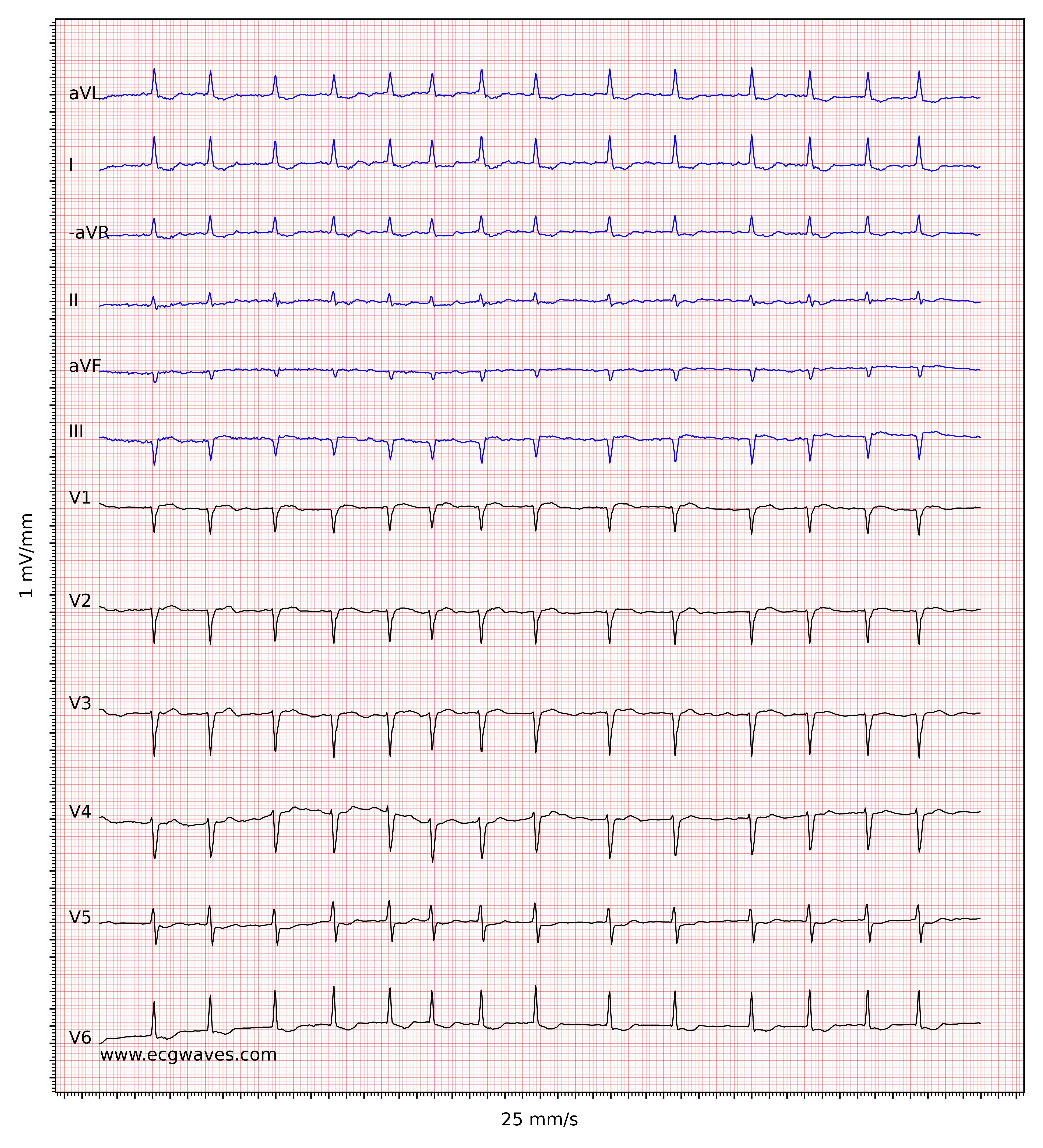
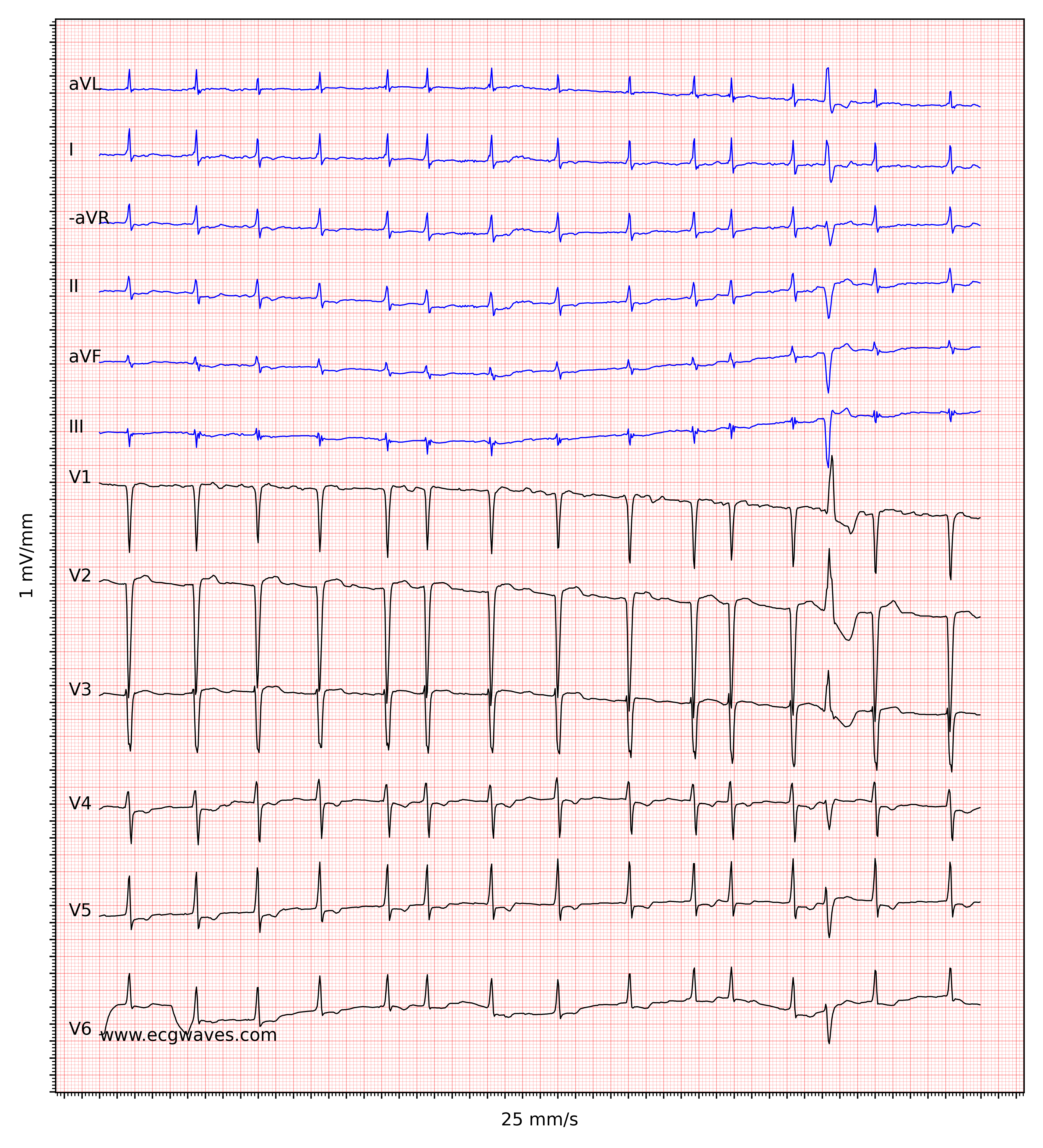
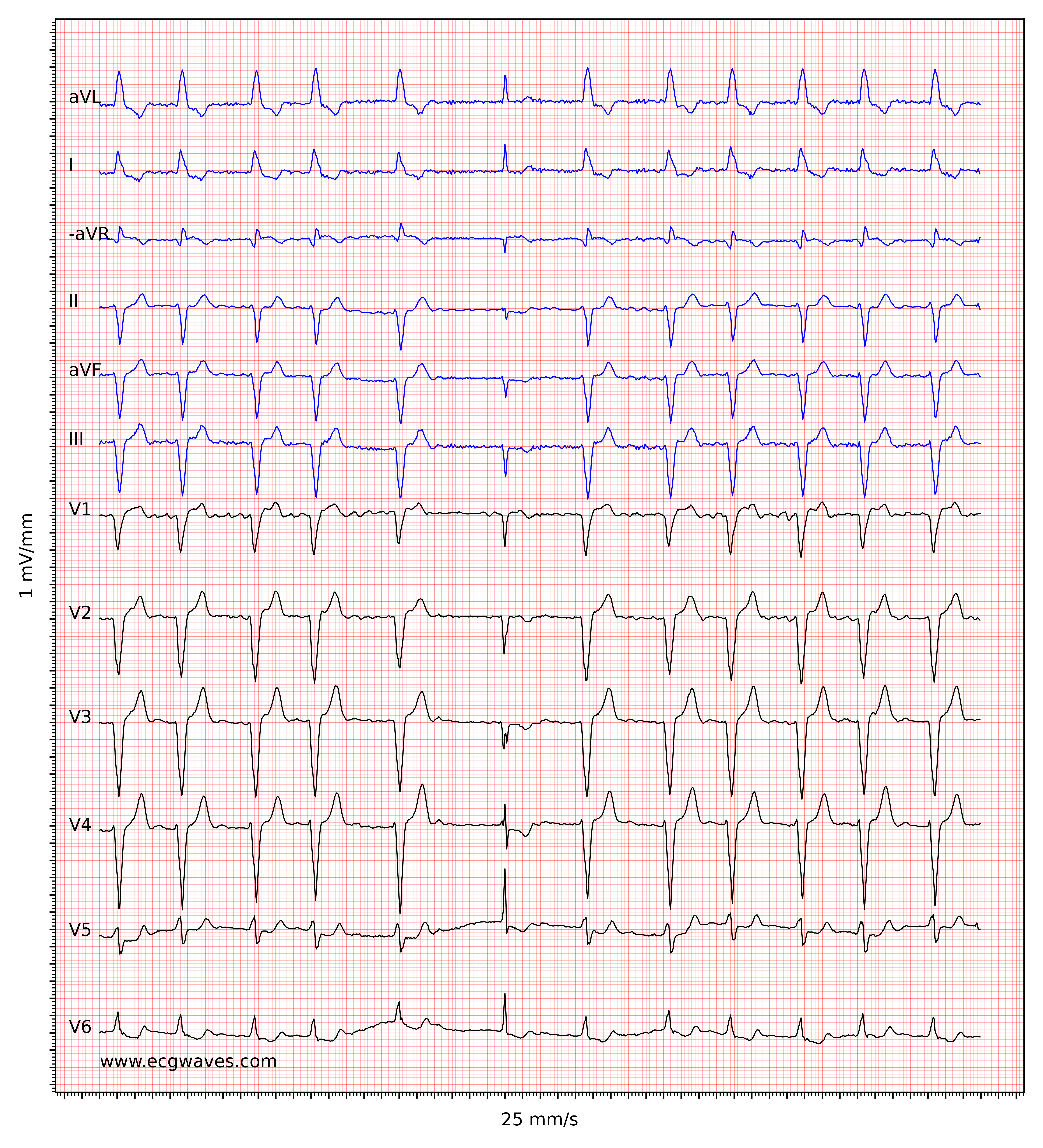
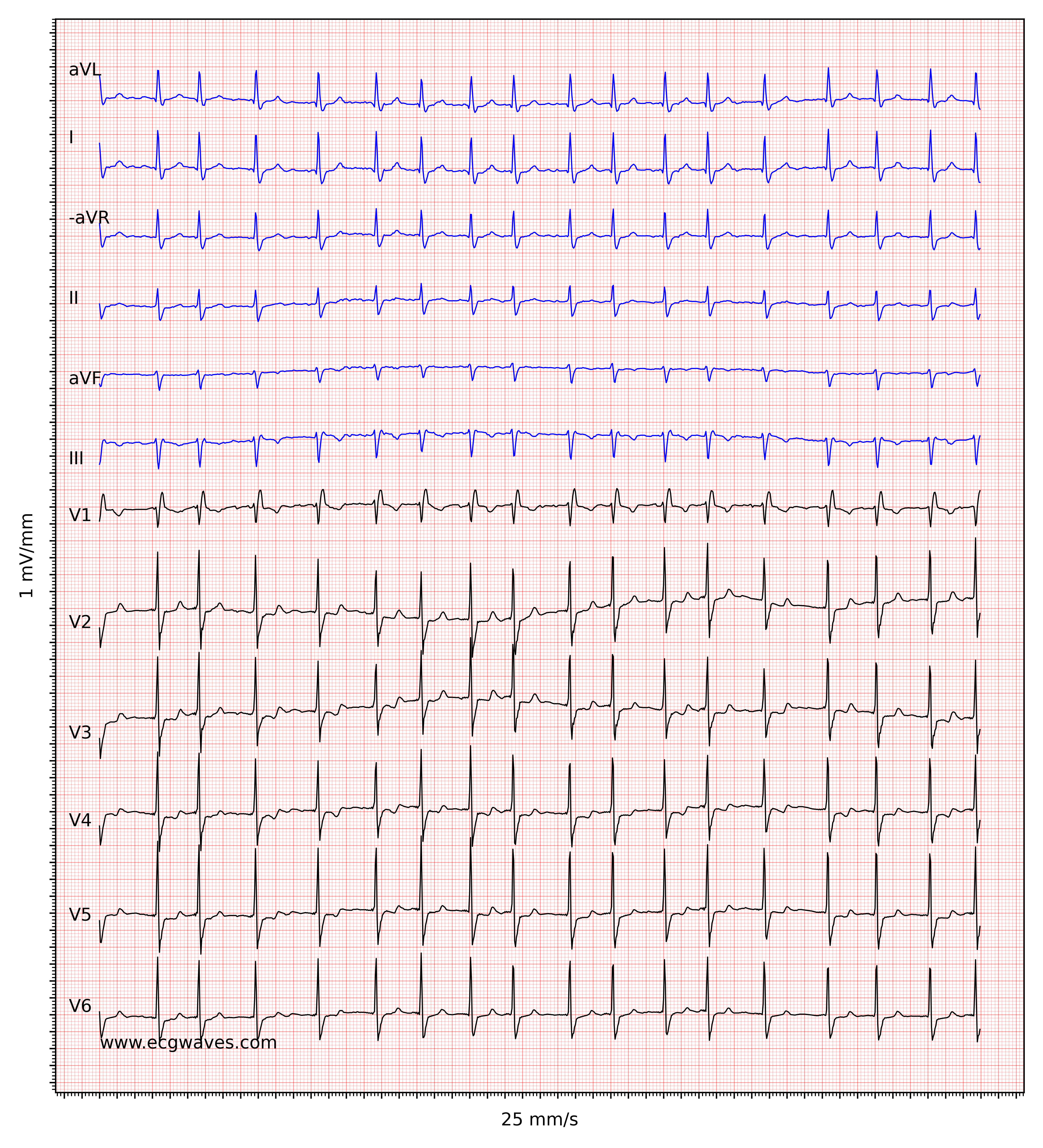
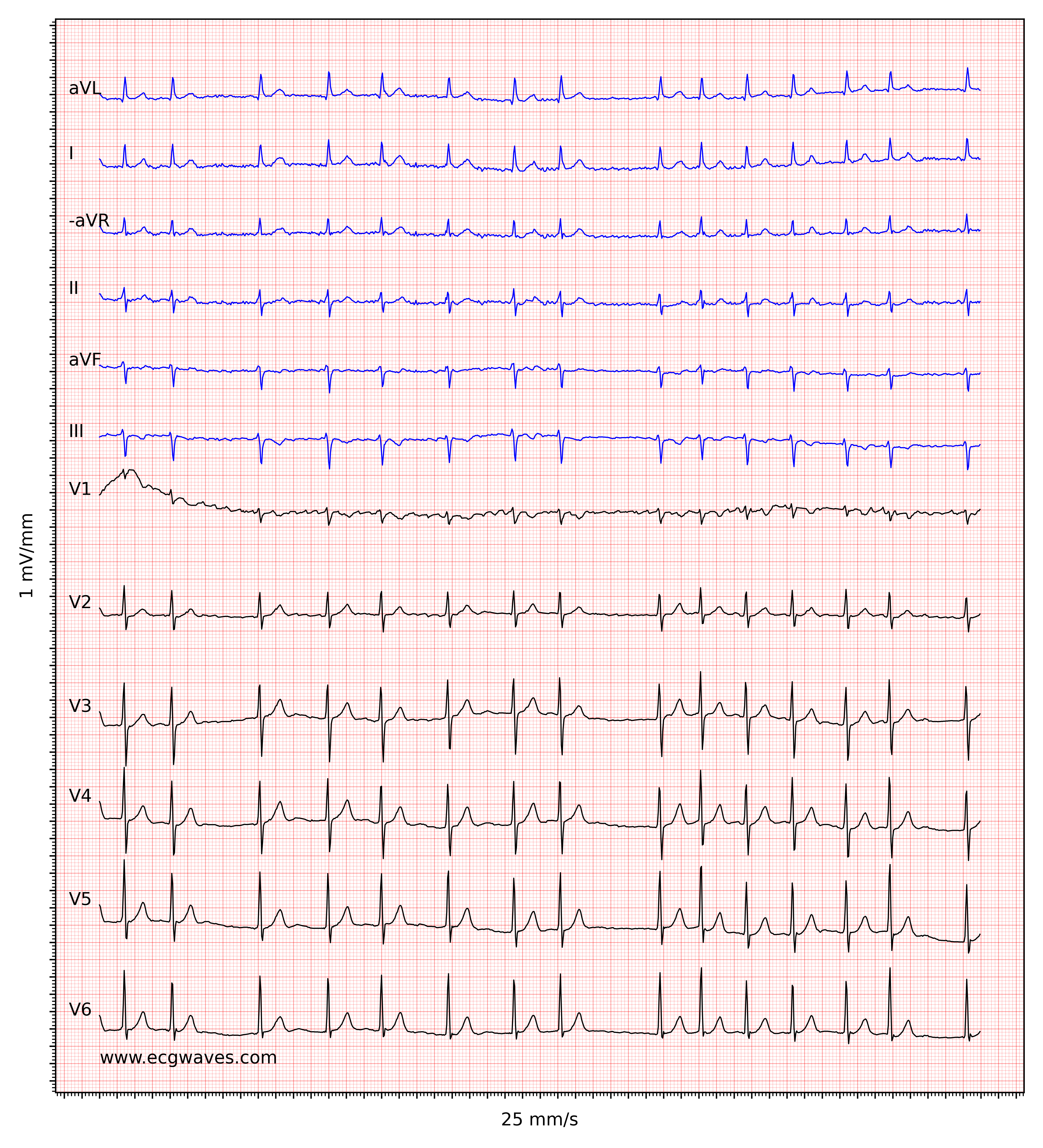
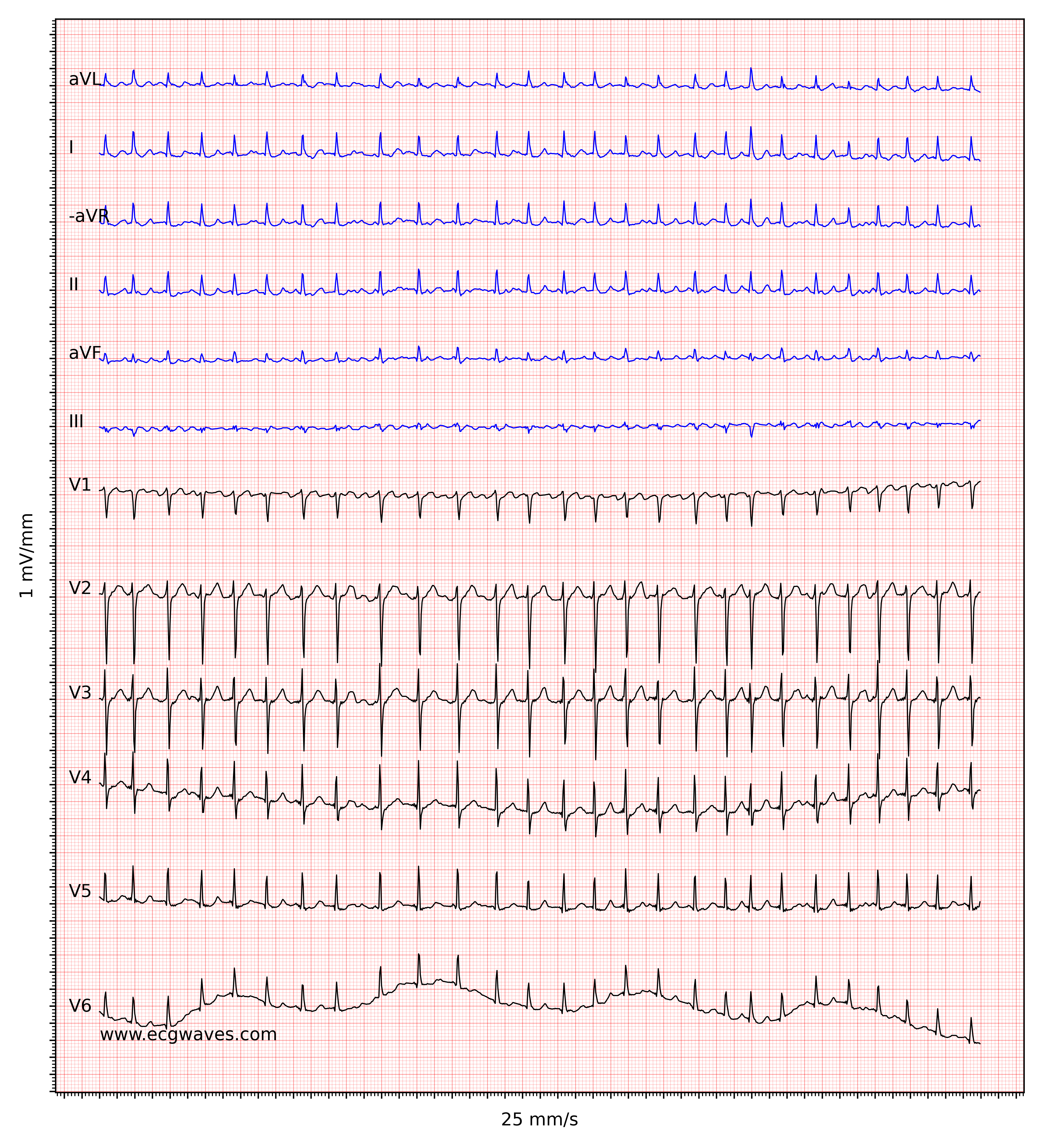
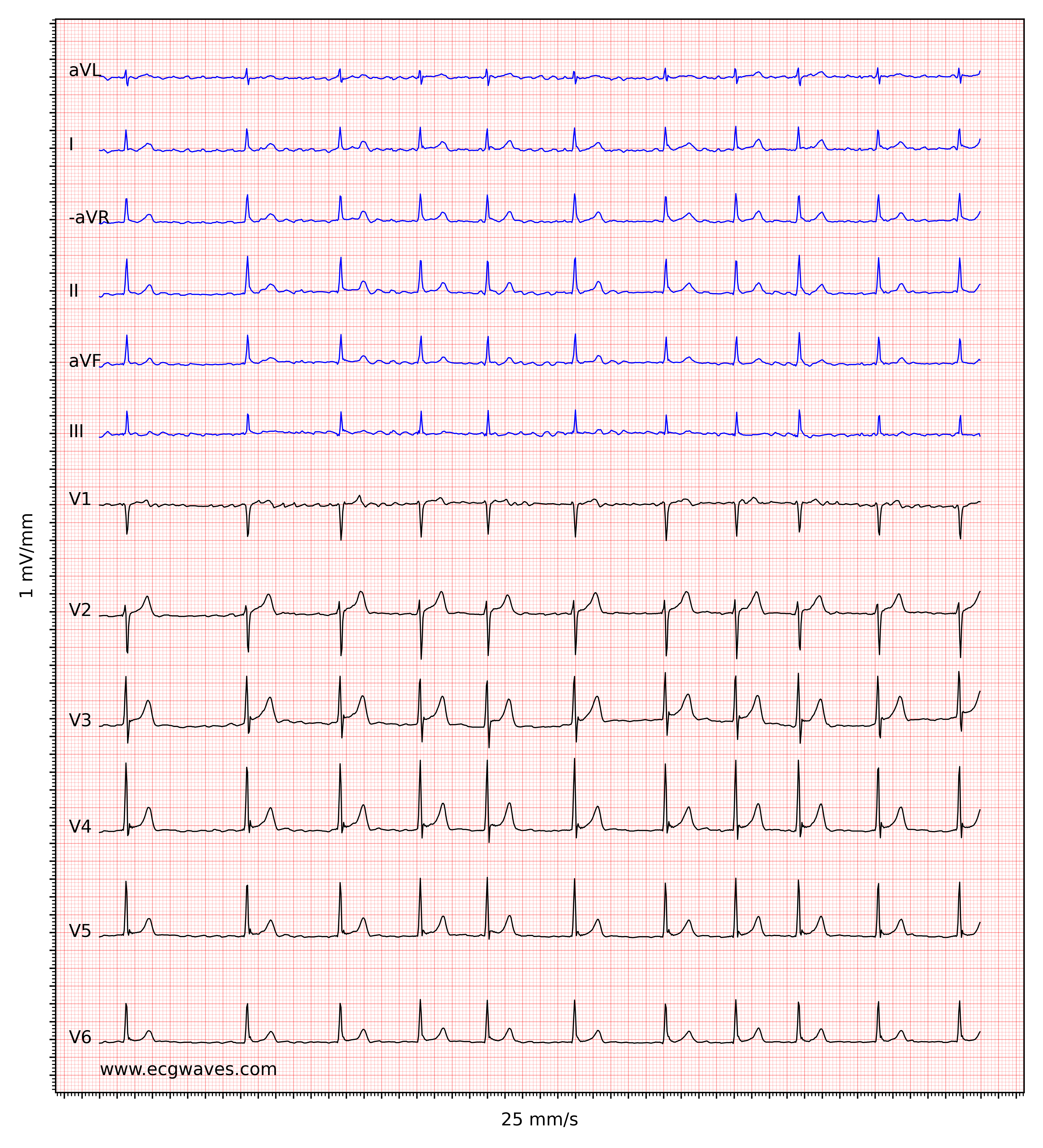
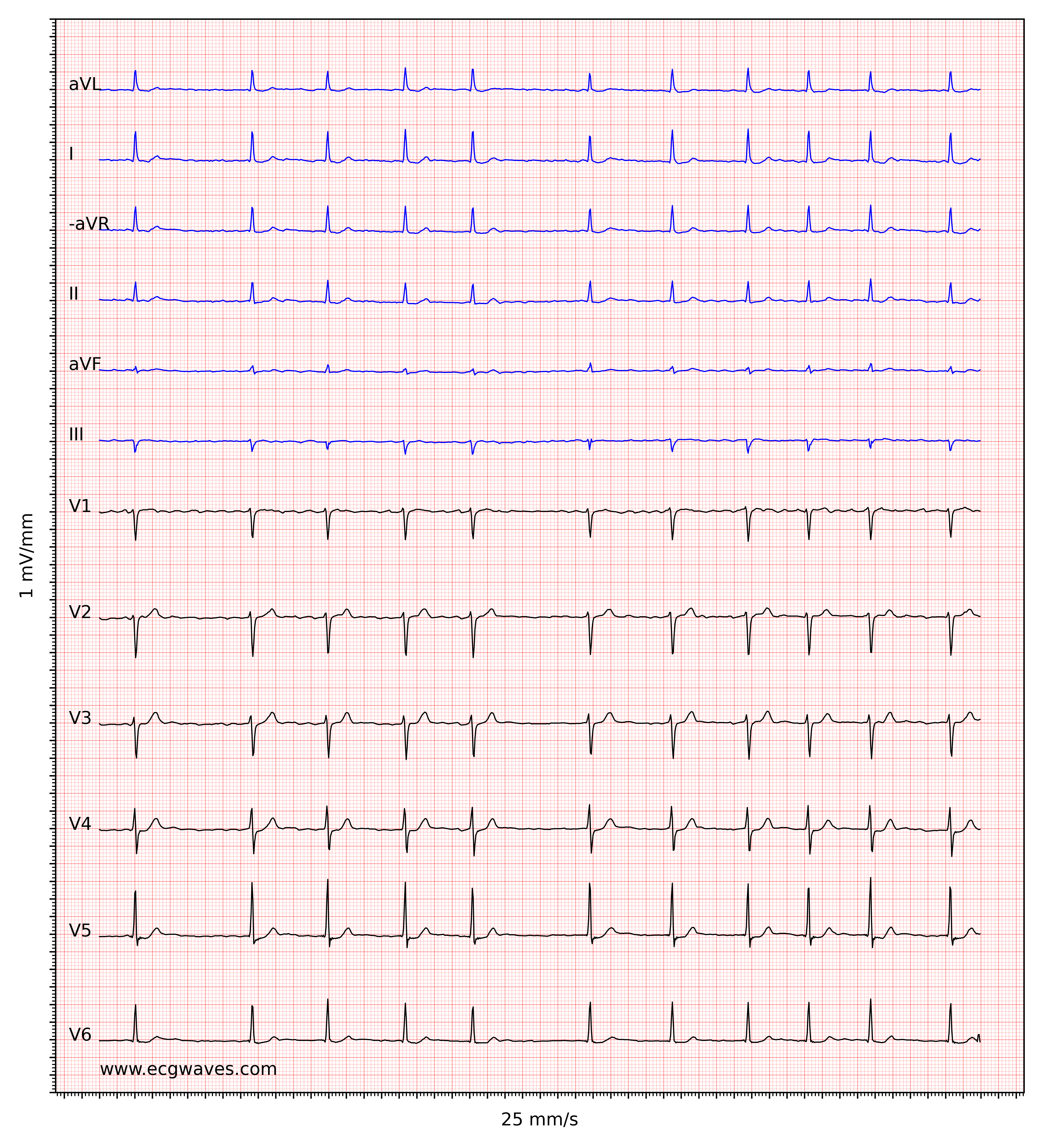
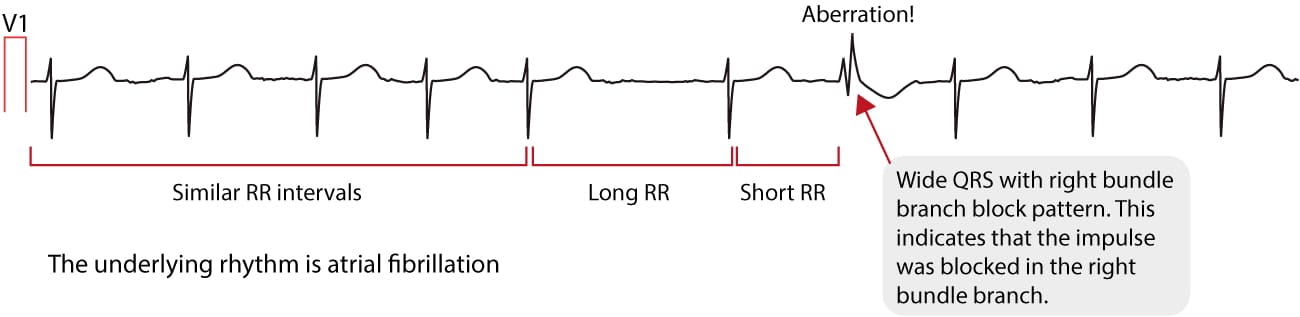
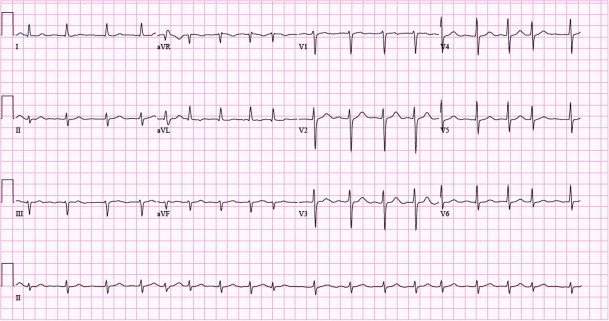
Kendetegnende for atrieflimren er fraværet af P-bølger og en uregelmæssig (dvs. helt uregelmæssig) ventrikelfrekvens. Basislinjen (den isoelektriske linje mellem QRS-komplekserne) er kendetegnet ved enten fibrillatoriske bølger (f-bølger) eller blot små svingninger. Fibrillatoriske bølger er små med varierende morfologi og høj frekvens (300 til 600 bølger pr. minut). Amplituden af f-bølger kan variere fra lille til stor. Store f-bølger må ikke forveksles med fladderbølger (F-bølger), som ses ved atrieflagren. Det er heldigvis let at skelne mellem disse to, fordi f-bølger altid har varierende morfologi, mens flutterbølger er mere eller mindre identiske (f-bølger har også højere frekvens end flutterbølger). Figur 1 og 2 viser EKG-eksempler på atrieflimren.
Ventrikelfrekvensen er helt uregelmæssig, typisk i området 100 til 180 slag pr. minut. Patientens alder, nuværende medicinering og samtidige AV-blokke ændrer ventrikelfrekvensen. Atrieflimren med meget hurtig ventrikelfrekvens kan se ud som en regelmæssig rytme (hvilket endnu er en grund til at skifte fra 25 mm/s til 50 mm/s papirhastighed), og derfor er det vigtigt omhyggeligt at måle rytmens regelmæssighed. Se EKG i figur 3. I tvivlstilfælde er det generelt sikkert at anvende carotis-massage, som øger den vagale aktivitet til atrioventrikulærknuden og dermed øger blokeringen i atrioventrikulærknuden; dette sænker ventrikelfrekvensen og gør uregelmæssigheden mere tydelig.
Atrieflimren klassificeres efter varigheden af arytmien.
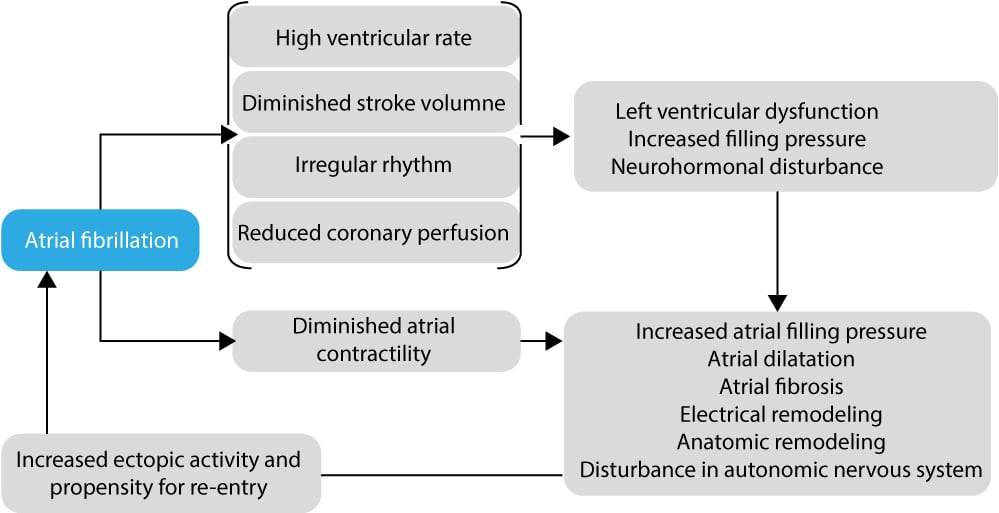
De anatomiske og elektrofysiologiske mekanismer, der forårsager atrieflimren, er stadig under udforskning. De underliggende mekanismer er noget komplicerede (diskuteres i detaljer nedenfor). For dem, der ikke er interesseret i elektrokardiologi, er det tilstrækkeligt at vide, at atrieflimren skyldes elektrisk kaos i forkamrene. Kaosset skyldes den samtidige eksistens af flere re-entry-kredsløb, som genererer impulsbølger, der forplanter sig gennem atrierne. Disse impulsbølger kolliderer med hinanden og med refraktære celler, hvilket fragmenterer bølgerne og skaber yderligere kaos. Interesserede læsere kan fortsætte med at læse den detaljerede forklaring på dette.Den lange historie
Atrieflimren er afhængig af to mekanismer: en trigger og en driver. Udløseren er den begivenhed, der starter atrieflimren, og driveren er den mekanisme, der opretholder arytmien. Atrierne hos personer, der udvikler atrieflimren, har elektrofysiologiske og anatomiske egenskaber, der fremmer triggere og drivere. Aldring, som er den stærkeste risikofaktor for atrieflimren, fører til degeneration af myokardiet og ledningscellerne. Andre risikofaktorer, såsom strukturel hjertesygdom (kardiomyopati, hjertesvigt, valvulær sygdom), iskæmisk hjertesygdom, lungesygdom, genetisk disposition, autonom dysfunktion osv. er andre risikofaktorer, der fremmer triggere og drivere. Undersøgelser viser entydigt, at de fleste triggere og drivere stammer fra lungevenerne, der tømmer iltet blod ind i venstre atrium.Overgangen mellem lungevenerne og atriets myokardium ser ud til at være elektrisk sårbar, og undersøgelser viser, at størstedelen af patienterne med paroxysmal atrieflimren har en trigger fra en lungevene. Triggeren består af et ektopisk fokus, som udleder impulser med en høj hastighed. Disse impulser kan fremkalde korte udbrud af atrieflimren, men medmindre der er etableret en driver, vil flimren ophøre, når triggeren holder op med at udlede impulser. En driver kan etableres, hvis impulserne, der spredes fra triggeren, møder myokardiet med varierende ledningsevne eller excitabilitet. Når impulsen møder et område med varierende ledningsevne/ekscitabilitet, kan der opstå re-entry på grund af blokering af impulsen. Nye impulsbølger vil sprede sig fra re-entry, og disse bølger kan kollidere med andre impulsbølger og enten blive afbrudt eller støde på nye blokke, som fragmenterer impulsen. Fragmentering af impulsen vil få resterne til at sprede sig på en tilfældig måde gennem forkamrene. Sammenfattende udløses paroxysmal atrieflimren af en trigger, der udleder impulser med høj frekvens; impulserne kan støde på myokardiet med heterogen eller varierende ledningsevne/excitabilitet, som kan fungere som en blok, der giver anledning til re-entry-kredsløb. Disse re-entry-kredsløb skaber yderligere re-entry-kredsløb.Tidlige faser af atrieflimren (dvs. paroxysmal og nydiagnosticeret atrieflimren) er karakteriseret ved at have et eller nogle få ektopiske foci. Et sådant fokus eller foci kan lokaliseres og elimineres ved hjælp af ablationsbehandling. Dette er generelt en kur mod atrieflimren, fordi eliminering af triggeren vil fjerne den oprindelige årsag. Antallet af ektopiske foci og antallet af genererede re-entry-kredsløb øges dog gradvist med tiden, og dette korrelerer stærkt med udviklingen til vedvarende og langvarigt vedvarende atrieflimren. Af samme grund er ablationsbehandling mindre effektiv hos personer med persisterende eller langvarigt persisterende atrieflimren.Forklaringen på, at antallet af ektopiske foci og re-entry-kredsløb stiger, er, at atrieflimren (og de risikofaktorer, der ledsager den) fremkalder elektrofysiologiske og anatomiske ændringer i atrierne, og disse ændringer fremmer triggere og drivere. Denne gradvise udvikling af atriets myokardium kaldes atrial remodeling. Graden af atrial remodeling korrelerer stærkt med antallet af episoder med atrieflimren. Blandt ændringerne i atrierne er f.eks. ændringer i ekspressionen og funktionen af ionkanaler (især calciumkanaler) og udviklingen af fibrose. I sidste ende bliver den funktionelle og anatomiske struktur i atrierne så omdannet, at atrieflimren bliver permanent.Udover lungevenerne kan ektopiske foci lokaliseres ved indgangen til vena cava superior, vena cava inferior, sinus coronarius og tilhæftningen af Marshalls vene.Det autonome nervesystem ser ud til at have en vigtig rolle i fremkaldelsen af paroxysmal atrieflimren. En tredjedel af alle personer med paroxysmal atrieflimren oplever deres episoder i situationer med høj vagal aktivitet (under søvn, i hvile) eller høj sympatisk aktivitet (under træning, stress osv.). Det autonome nervesystem ændrer aktionspotentialerne i atriets myokardium, især omkring lungevenerne. Den autonome innervation af atrierne er dog ikke homogen (spredningen af autonome fibre i atrierne varierer), hvilket betyder, at effekten på aktionspotentialerne heller ikke er homogen, og det fremmer atrieflimren.Selvom atrieflimren i de fleste tilfælde udløses af et ektopisk fokus, kan den også udløses af andre arytmier som AVRT eller atrieflagren eller endda bradykardi. Sidstnævnte (bradykardi) menes at forårsage atrieflimren, fordi ektopiske fokusser ved lave hjertefrekvenser kan komme til udtryk, når de ikke undertrykkes af sinoatrialknuden.Undersøgelse af atrieflimrenAtrieflimren bekræftes ved hjælp af forskellige elektrokardiografiske metoder, herunder hvile-EKG, Holter-EKG og event recorder. Holter-EKG er især nyttigt til at vurdere hyppigheden og varigheden af arytmiepisoder, herunder asymptomatiske episoder. De diagnostiske kriterier for atrieflimren baseret på elektrokardiografiske fund er som følger:
Ekkokardiografi anbefales til alle patienter med nydiagnosticeret atrieflimren.NT-pro-BNP-niveauer kan måles, hvis der er mistanke om hjertesvigt.Behandling af atrieflimren
Behandling af akut atrieflimren– Undgå forsøg på kardioversion hos patienter med stærkt nedsat uddrivningsfraktion i venstre ventrikel. Konvertering til sinusrytme hos sådanne patienter kan føre til en lavere hjertefrekvens og en betydelig reduktion af hjertets output, hvilket potentielt kan resultere i kardiogent shock.
– For patienter, der ikke får antikoagulantia, eller som får subterapeutiske doser, anbefalede tidligere retningslinjer et 48-timers vindue for forsøg på kardioversion. I 2024 reviderede European Society of Cardiology (ESC) imidlertid denne anbefaling og forkortede vinduet til maksimalt 24 timer for forsøg på kardioversion.
Cirka 60 % af tilfældene af akut atrieflimren vil spontant konvertere til sinusrytme inden for 16 timer efter symptomdebut. Hvis der ikke er tegn på kredsløbskompromittering, kan man forvente, at situationen er sådan i 24 timer (regnet fra symptomdebut), indtil kardioversion forsøges. Hvis man planlægger at udføre kardioversion, skal det ske inden for 24 timer fra symptomdebut. Kardioversion er kontraindiceret efter 24 timer på grund af den høje risiko for tromboemboli (medmindre der kan udføres et transesofagealt ekkokardiogram for at udelukke trombedannelse i atrierne (venstre atrial appendage)). Elektrisk kardioversion er den mest effektive metode og giver en succesrate på >90% med bifasisk stød ≥120 J. Farmakologisk kardioversion (flecainid, propafenon, ibutilid, amiodaron, vernakalant) er mindre effektiv (ca. 75% succesrate), og disse antiarytmiske lægemidler kan forårsage arytmier samt kredsløbskompromittering på grund af negativ inotropisk effekt. Ikke desto mindre er elektrisk kardioversion det sikreste behandlingsalternativ ved enhver arytmi.Gentagen administration af intravenøse betablokkere, digoxin eller calciumkanalblokkere kan være nødvendig for at sænke ventrikelfrekvensen. Det er klogt at starte med betablokkere og derefter give digoxin, hvis betablokkere er utilstrækkelige.Man skal straks tage stilling til, om patienten har behov for antikoagulantia, og de fleste patienter bør indlægges med en dosis lavmolekylært heparin (LMWH), indtil der er truffet en beslutning om antikoagulation.Langtidsbehandling af atrieflimrenHastighedskontrol af atrieflimren (kontrol af ventrikelfrekvensen)Den hurtige ventrikelfrekvens under atrieflimren er en af hovedårsagerne til den øgede dødelighed, der observeres hos personer med atrieflimren. Hastighedskontrol indebærer, at ventrikelfrekvensen er målet for behandlingen. Målet er at sænke ventrikelfrekvensen så meget som muligt uden at fremprovokere overdreven bradykardi. Hastighedskontrol opnås med medicin, der påvirker AV-knuden; mere specifikt sænker disse lægemidler overledningen gennem AV-knuden, og det resulterer i, at færre atrieimpulser ledes til ventriklerne. Betablokkere (propranolol, metoprolol, atenolol, esmolol, nadolol), calciumkanalblokkere (diltiazem, verapamil) og digoxin (digitalis) er fremragende valg til at sænke ventrikelfrekvensen. Sotalol er forbeholdt kardiologer, da det også har pro-arytmiske effekter. Hastighedskontrol er ikke ringere end rytmekontrol med hensyn til overlevelse. Det kan anbefales at sigte mod en ventrikelfrekvens på under 100 slag i minuttet. Detaljer om medicin og dosering følger i tabel 1.Rytmekontrol af atrieflimren: medicin, der nedsætter overledningen gennem AV-knuden
| MEDICIN | FORDELE | ULEMPER | DOSERING | BEGYNDENDE VIRKNING | ELIMINATIONSHALVERINGSTID | |
|---|---|---|---|---|---|---|
| BETA-BLOKERE | ||||||
| Propranolol | Hurtig indsættende virkning, kort virkningsvarighed for intravenøse former; pulskontrol i hvile og ved aktivitet; der findes orale former med varierende virkningsvarighed | Kan forværre hjertesvigt hos dekompenserede patienter; kan forværre reaktive luftvejssygdomme; kan forårsage træthed, depression; pludseligt ophør kan forårsage rebound-takykardi, hypertension | – IV: 1 mg gives som bolus, gentag q5min efter behov for at opnå målet – Oral: 10-30 mg/dosis hver 6.-8. tid | – IV: virkningens indtræden inden for 5 minutter – Oral: virkningens indtræden inden for 1-2 timer | – IV: virkningens varighed er 30-60 minutter – Oral: 3-5 timer | |
| Metoprolol | Samme som propranolol. | Samme som propranolol. | – IV: 2,5-5 mg over 2-3 min, gentag q5min efter behov for at opnå målet – Oral: 12,5-100 mg/dosis hver 6.-8. tid – Præparater med vedvarende frigivelse fås til dosering én gang dagligt | – IV: virkningens indtræden inden for 5 minutter – Oral: virkningens indtræden inden for 1-2 timer | – IV: virkningens varighed er 30-60 minutter – Oral: 3-6 timer | |
| Atenolol | Samme som propranolol. | Samme som propranolol. | – IV: 5 mg over 5 min, gentag q10min for at opnå målet – Oral: 25-100 mg/dosis q8-12hr | – IV: virkningens indtræden inden for 5 minutter – Oral: virkningens indtræden inden for 1-2 timer | – IV: virkningens varighed er 30-60 minutter – Oral: 6-9 timer | |
| Esmolol (kun intravenøs) | Samme som propranolol. | Samme som propranolol. | – IV: 500 µg/kg over 1 min, derefter vedligeholdelsesdosis på 25-300 µg/kg/min; titreres med 25-50 µg/kg/min hver 5.-10. minut for at opnå målet | – IV: indsættende virkning inden for 5 min | N/A | |
| Nadolol (kun oral) | Samme som propranolol. | Samme som propranolol. | – Oral: 40-80 mg dagligt i starten; øg til 240-320 mg dagligt efter behov for at nå målet; kan give én gang dagligt | – Oral: virkningens indtræden inden for 1-2 timer | 14-24 timer | |
| CALCIUMKANALBLOKKERE | ||||||
| Diltiazem | Samme som for betablokkere | Kan forværre hjertesvigt hos dekompenserede patienter; kan forårsage træthed; pludselig seponering kan forårsage rebound-takykardi, hypertension | – IV: 0,25 mg/kg over 2 min , derefter infusion med 5-15 mg/time i op til 24 timer; gentagen bolus på 0,35 mg/kg kan være nødvendig – Oral: 30-120 mg/dosis hver 6.-8. time; præparater med vedvarende frigivelse fås som doser én eller to gange dagligt | – IV: virkningens indtræden inden for 5 minutter – Oral: begyndende virkning inden for 1 gang | 5-7 timer | |
| Verapamil | Samme som for betablokkere | Kan forværre hjertesvigt hos dekompenserede patienter; kan forårsage træthed; abrupt seponering kan forårsage rebound-takykardi, hypertension | – IV: 5- til 10-mg bolus q15-30min for at opnå målet – Oral: 80-120 mg dosis hver 8.-12. time; præparater med vedvarende frigivelse fås som doser én eller to gange dagligt | – IV: virkningens indtræden inden for 5 minutter – Oralt: virkningens indtræden inden for 1 gang | 5-12 t | |
| ANDRE | ||||||
| Digoxin (digitalis) | Kan bruges til patienter med hjertesvigt | Langsomt indsættende virkning; dårlig kontrol af hjertefrekvens med aktivitet; snæver terapeutisk margin; lang virkningsvarighed | IV-ladningsdosis på op til 1,0 mg i de første 24 timer, med bolus på 0,25-0,5 mg IV-push; derefter resten i opdelte doser 16-8 timer; oral vedligeholdelsesdosis, 0,125-0,25 mg hver dag | – IV: op til 30 minutter – Oral: 2-4 timer | 36 timer |
Antikoagulation som profylakse mod tromboembolisme
Slagtilfælde, forbigående iskæmiske anfald og perifere embolier er almindelige ved atrieflimren og skal behandles. Risikoen for tromboemboli er ikke, som man tidligere har troet, lige stor ved alle tidligere for atrieflimren. En nylig metaanalyse af Ganesan et al. viste, at paroxysmal atrieflimren er forbundet med en lavere risiko for slagtilfælde end vedvarende atrieflimren. Fordelene ved antikoagulation er dog de samme i de to grupper, og begge bør behandles med de samme algoritmer. De nuværende retningslinjer for antikoagulation ved atrieflimren indeholder således ingen specifikke råd i forhold til typen af atrieflimren.
Begynd med at bedømme risikoen for tromboemboli ved hjælp af CHADS-score og/eller CHADS-VA-score. Blødningsrisikoen bør vurderes ved hjælp af HAS-BLED-score. Patienter med større risiko for tromboemboli end for blødning bør tilbydes antikoagulation. Risikoen for slagtilfælde reduceres med 70 % ved brug af billig antikoagulantia som warfarin. Nyere muligheder (dabigatran, apixaban, rivaroxaban) er dyrere, lige så effektive til at reducere slagtilfælde, kræver ikke overvågning af PK/INR og ser ud til at forårsage færre alvorlige blødninger.