Introduktion til hjertestimulering og enheder: Pacemaker, ICD, CRT
Den kunstige pacemaker er en af de store medicinske opfindelser i det 20. århundrede. Hjertestimulering har udviklet sig fra et farligt eksperiment i 1930’erne til en rutinemæssig, sikker og sofistikeret behandling, der bruges over hele verden. Kunstige pacemakere har haft stor gavn af tekniske fremskridt, især med fremkomsten af transistorer, programmerbare kredsløb, litiumbatterier og internetforbundne enheder. Der er sket yderligere gennembrud i de senere år, hvor den blyfri pacemaker er den mest lovende forbedring.1
I betragtning af den udbredte brug af pacemakere og tendensen til øget brug af hjerteudstyr generelt er det vigtigt at kende til disse apparater. Dette afsnit handler om kunstige pacemakere. Mere avanceret udstyr (ICD, implanterbar kardioverterdefibrillator; CRT, kardial resynkroniseringsterapi) diskuteres i de efterfølgende kapitler. Den første del består af en kort repetition af det grundlæggende i hjertets automatik, aktionspotentialer og pacemakerceller.
Principper for myokardiets excitabilitet og ledningssystem
For at opnå en effektiv pumpemekanisme skal atrierne og ventriklerne aktiveres hurtigt og sekventielt. Hurtig aktivering er vigtig for at aktivere så meget myokardie som muligt på samme tid; jo mere myokardie, der trækker sig sammen på samme tid, jo mere effektiv er pumpemekanismen. Sekventiel aktivering betyder, at forkamrene aktiveres først og fylder ventriklerne med tilstrækkelige mængder blod, før ventriklerne begynder at trække sig sammen. For at koordinere disse to opgaver har hjertet en iboende pacemaker – dvs. sinusknuden – og et elektrisk ledningssystem, der består af specialiserede myokardieceller. Ledningscellerne danner bundter af fibre, som spreder aktionspotentialet hurtigt og sekventielt til det kontraktile myokardium. Når det kontraktile myokardium modtager aktionspotentialet, aktiveres det og trækker sig sammen. Figur 1 illustrerer sinusknuderne og komponenterne i ledningssystemet.
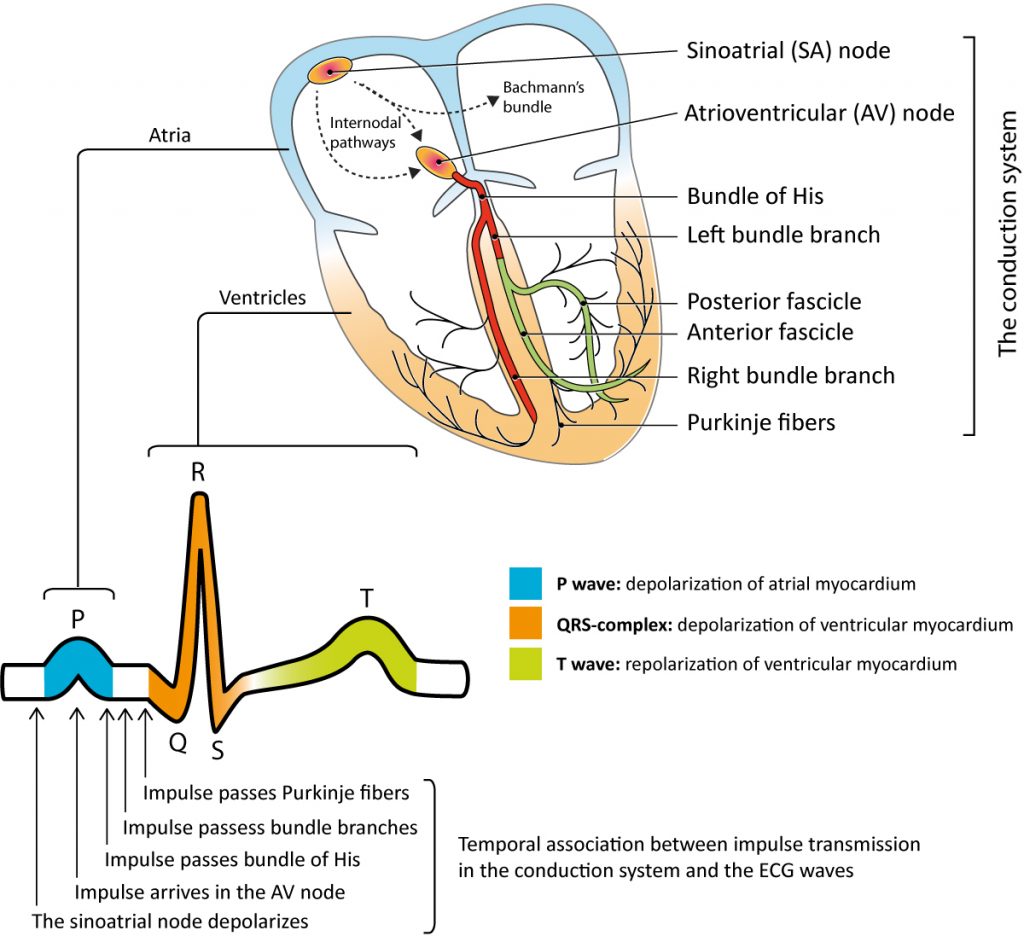
AV-systemet består af AV-knuden, His-bundtet og Purkinje-fibrene. Disse strukturer overfører atriepulsen til ventriklerne. Impulsoverførslen er hurtig gennem His-bundtet og Purkinje-fibrene, så stort set hele det ventrikulære myokardium aktiveres (depolariseres) samtidig. Den hurtige aktivering af ventriklerne giver et smalt QRS-kompleks (defineret som QRS-varighed <120 ms).
Hjertets aktionspotentiale
Aktionspotentialet omfatter en depolarisering (aktivering) efterfulgt af en repolarisering (gendannelse). Hjertets cyklus starter, når sinusknuden udleder det første aktionspotentiale, som derefter spreder sig gennem myokardiet som en bølgefront i vand. Figur 2 viser, hvordan aktionspotentialet ser ud i kontraktile myokardieceller.
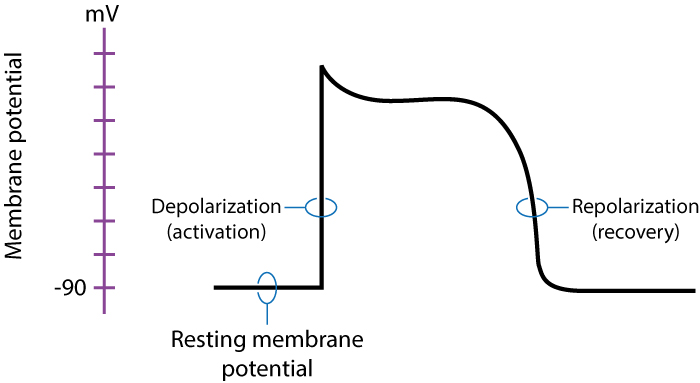
Hjertets elektromekaniske kobling
Depolarisering aktiverer myokardiecellerne og inducerer cellulære processer, der fører til cellesammentrækning. Udbredelsen af en elektrisk impuls er derfor direkte koblet til en mekanisk begivenhed; dette kaldes elektromekanisk kobling.
Det elektriske ledningssystem i hjertet
Sinusknuden (sinoatrialknuden) og intrinsisk automatik
Sinusknuden er en lille oval struktur, der ligger nær indgangen til vena cava superior i højre atrium (Figur 1). Sinusknuden består af højt specialiserede celler, der har en unik evne til at depolarisere spontant. Cellerne i sinusknuden er således i stand til spontant at udløse et aktionspotentiale. Denne evne kaldes automatik. Cellerne i sinusknuden har en iboende depolariseringshastighed på ca. 70 gange i minuttet, hvilket resulterer i 70 sammentrækninger i minuttet. Sinusknuden er hjertets primære pacemaker.
Sekundære (latente) pacemakere
Der er yderligere strukturer, som har automatik og dermed evne til at fungere som hjertets pacemaker. Disse strukturer er som følger:
- Dele af det atriale myokardium: Der er klynger af atriale myokardieceller placeret omkring crista terminalis, indgangen til sinus coronarius og vena cava inferior samt celler omkring mitral- og tricuspidalklapperne, som besidder automatik. Disse celler er ikke ledningsceller i sig selv; de er faktisk kontraktile celler, der besidder automatik. Automatikken er altså ikke forbeholdt cellerne i ledningssystemet.
- Celler, der omgiver den atrioventrikulære (AV) knude: Det er en almindelig misforståelse, at den atrioventrikulære (AV) knude besidder automatik, fordi der ikke er noget overbevisende bevis for det. Der er dog tegn på, at celleklynger omkring AV-knuder besidder automatik.
- His-Purkinje-netværket: His-bundtet og hele Purkinje-netværket besidder automatik.
Hjertet har således fire pacemakere (sinusknuden, dele af atriemyokardiet, myokardiet omkring AV-knuden og His-Purkinje-netværket). Grunden til, at sinusknuden er den primære pacemaker, er ganske enkelt, at den har den højeste iboende hastighed af spontan depolarisering (dvs. den hurtigste automatik). Hjerterytmen styres af den hurtigste pacemaker, fordi denne pacemaker vil depolarisere før de konkurrerende pacemakere og nulstille dem.
Den iboende depolariseringshastighed for alle pacemakerceller er afbildet i figur 3.
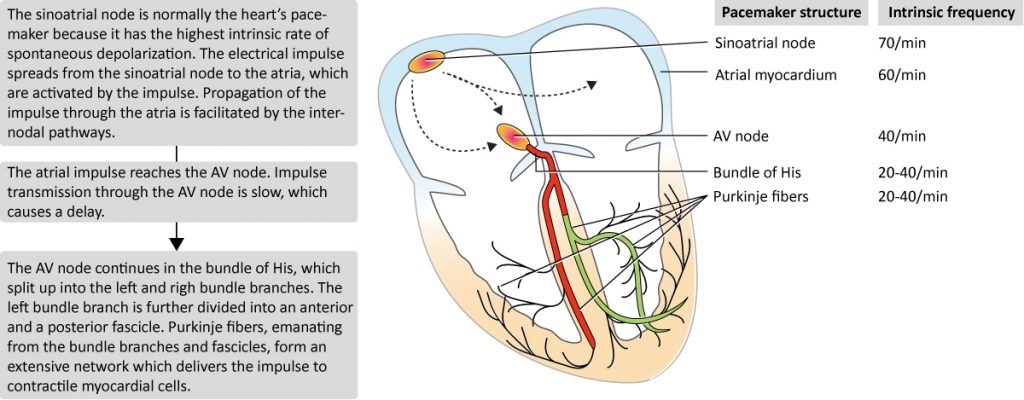
Kunstige pacemakere
Hvis sinusknuden ikke kan generere impulser, eller hvis det elektriske ledningssystem ikke kan overføre impulser, kan det føre til bradykardi eller endda asystoli. Latente pacemakere forhindrer typisk asystoli ved at etablere en flugtrytme. Selv om sådanne flugtrytmer kan være livreddende, har de to grundlæggende mangler:
- Escape-rytmer etableret af latente pacemakere har en lavere frekvens end sinusknuden, hvilket betyder, at hjertets minutvolumen reduceres.
- Escape-rytmer etableret af latente pacemakere er upålidelige på lang sigt, fordi deres aktivitet kan ophøre helt, hvilket resulterer i asystoli.
Kunstige pacemakere er indiceret, hvis impulsdannelsen eller impulsledningen er defekt, så der udvikles bradykardi. Den mest almindelige årsag til defekt impulsdannelse er sinusknudedysfunktion, og den mest almindelige årsag til defekt impulsledning er AV-blok.
Selv om slagvolumen øges en smule under bradykardi (på grund af øget fyldningstid), resulterer det i nedsat minutvolumen. Hvis hjertets minutvolumen falder betydeligt, opstår der symptomer som svimmelhed, presynkope eller endda synkope. Hvis hjertets minutvolumen er nedsat, men den cerebrale perfusion er tilstrækkelig, kan der opstå dyspnø, træthed, træningsintolerance, ubehag i brystet eller hjertesvigt.
Fra et klinisk perspektiv er håndteringen mere presserende, hvis bradykardien skyldes AV-blok, hvilket skyldes, at AV-blok af høj grad (AV-blok afanden grad, AV-blok af tredje grad) kan forårsage asystoli.
Intrinsisk hjerteautomatik: Pacemaker-potentiale
Automatikken i cellerne i sinusknuden forklares ved, at disse celler begynder at lække natrium (Na ) ind i cellen, så snart de vender tilbage til deres hviletilstand (figur 4). Når natrium lækker ind i cellen, bliver cellemembranen gradvist mere positiv. Når membranpotentialet når sin tærskel på -40 mV, udløses aktionspotentialet, og cellen depolariseres. Ved -40 mV åbner spændingsstyrede calciumkanaler (Ca2 ), så calcium strømmer ind i cellen og forårsager depolarisering. Efterfølgende åbner udadrettede kaliumkanaler (K ), hvilket resulterer i repolarisering af cellen. Cyklussen gentager sig derefter. Lækagen af natrium i hvilefasen kaldes pacemakerpotentialet.
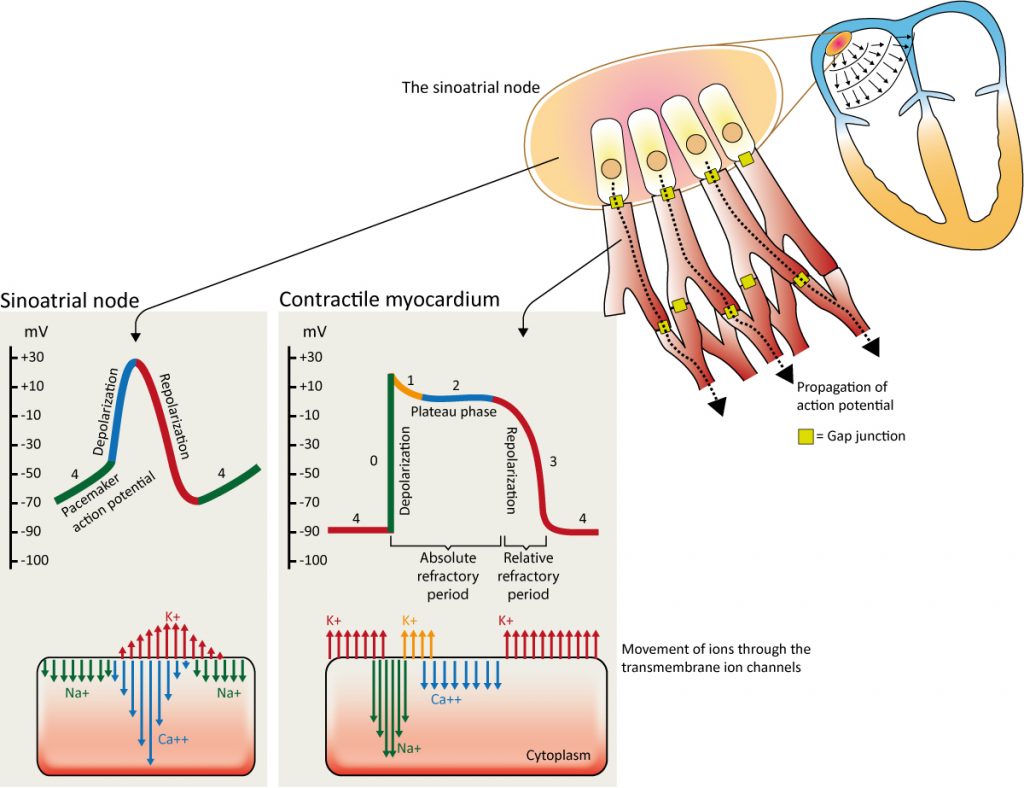
Depolariseringen spreder sig fra sinusknuden til det atriale og ventrikulære myokardium. Udbredelsen af aktionspotentialet er mulig, fordi alle hjerteceller er elektrisk forbundet med gap junctions (Figur 4). Tætheden af gap junctions i Purkinje-netværket er meget høj, hvilket forklarer den hurtige impulsoverførsel i netværket. Cellerne i den atrioventrikulære knude har derimod en meget lav tæthed af gap junctions, hvilket forklarer den langsomme impulsoverførsel gennem den atrioventrikulære knude. Overførslen af aktionspotentialet mellem kontraktile myokardieceller er også langsom på grund af de få gap junctions mellem dem.
De kontraktile celler har i modsætning til cellerne i sinoatrialknuden et ægte hvilepotentiale (fase 4), som er omkring -90 mV. Disse celler skal stimuleres for at fremkalde et aktionspotentiale. Ved stimulering åbnes natriumkanaler (Na ), hvilket medfører en hurtig indstrømning af natrium og depolariserer cellerne. Kontraktile celler begynder at trække sig sammen et par millisekunder efter depolariseringens start, og de begynder at slappe af et par millisekunder efter repolariseringen er afsluttet. Aktionspotentialets varighed er ca. 0,20 sekunder i det atriale myokardium og 0,3 sekunder i det ventrikulære myokardium (figur 4).
Læs mere om dette: Hjertets elektrofysiologi: aktionspotentiale, automatik og vektorer
Absolutte og relative refraktærperioder under aktionspotentialet
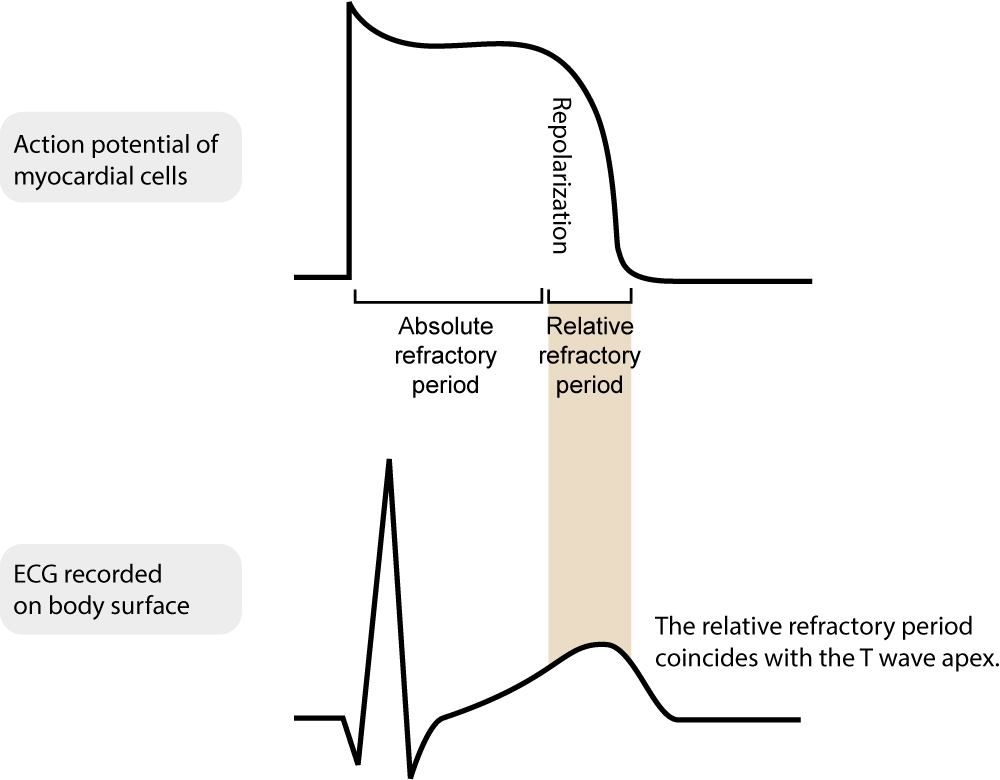
Under størstedelen af aktionspotentialet er myokardiecellen absolut refraktær over for stimulering, hvilket betyder, at en yderligere stimulus ikke kan udløse et nyt aktionspotentiale, uanset stimulusens intensitet. Den absolutte refraktærperiode efterfølges af en relativ refraktærperiode, hvor en stærk stimulering kan udløse et nyt aktionspotentiale. De absolutte og relative refraktærperioder er vist i figur 5.
Principper for kunstige pacemakere
Moderne pacemakere er ekstremt sofistikerede. De kan erstatte både impulsdannelse og impulsledning. De kan også tilpasse deres funktion til hjertets egen aktivitet (ved at registrere ) og til kroppens behov (ved at reagere på hjertefrekvensen). Moderne pacemakere kan også registrere og behandle takyarytmier, både supraventrikulære og ventrikulære. Disse emner og meget mere vil blive diskuteret i de efterfølgende kapitler.
Referencer
Reynolds et al. A Leadless Intracardiac Transcatheter Pacing System Liste over forfattere. The New England Journal of Medicine.
Mulpuru et al. Hjertepacemakere: Funktion, fejlfinding og håndtering. JACC.
