Lungeemboli opstår, når venøse blodpropper emboliserer til lungearterien eller dens forgreninger. I de fleste tilfælde dannes tromben i de dybe vener i benene eller bækkenet. Tromber dannet i de dybe vener i benene eller bækkenet kan løsne sig og strømme via vena cava inferior til højre atrium og ventrikel. Tromben pumpes fra højre hjertekammer gennem lungeklappen ind i hovedpulsåren. Afhængigt af trombens størrelse og form vil den okkludere hovedpulsåren eller dens forgreninger. Jo større tromben er, jo mere proksimal er okklusionen, og jo større er de hæmodynamiske effekter.
Okklusionen har to umiddelbare effekter:
- Nedsat perfusion i lungekredsløbet, hvilket resulterer i hypoxi.
- Reduceret preload i venstre ventrikel og dermed reduceret hjerteminutvolumen.
En betydelig reduktion i lungeperfusionen og den efterfølgende reduktion i venstre ventrikels preload fører til en kaskade af hæmodynamiske ændringer, som kan kulminere i hjertestop.
Lungeemboli er kausalt relateret til dyb venetrombose (DVT). Omkring 70 % af personer med symptomatisk lungeemboli har en igangværende DVT, og 30 % af personer med DVT har asymptomatisk lungeemboli (Di Nisio et al). Derfor overlapper risikofaktorer for lungeemboli med risikofaktorer for DVT; immobilisering, kirurgi, hyperkoagulabilitet og graviditet er almindelige risikofaktorer (se Risikofaktorer nedenfor).
En betydelig del af tilfældene med lungeemboli kræver trombolyse for at opløse okklusionen. Administration af trombolyse kræver omhyggelig overvejelse af absolutte og relative kontraindikationer (omtalt nedenfor) og vurdering af differentialdiagnoser; hjertetamponade, aortaaneurisme og aortadissektion er almindelige differentialdiagnoser, som udgør kontraindikationer for trombolyse.
Venøs tromboemboli er en kronisk og alvorlig tilstand. Dødeligheden ved lungeemboli er op til 20 %, og ca. 30 % af patienterne med lungeemboli eller dyb venetrombose oplever endnu en trombotisk hændelse inden for 10 år (Goldhaber et al., Kearon et al.).
Epidemiologi af lungeemboli
- Venøs tromboemboli (VTE) er den tredjestørste kardiovaskulære dødsårsag på verdensplan. Kun slagtilfælde og akut myokardieinfarkt er mere almindelige. Det svarer til, at der hvert år opstår 10 millioner tilfælde af venøs tromboemboli på verdensplan (Raskob et al).
- Forekomsten af lungeemboli er steget i de seneste årtier. Mulige forklaringer på denne tendens omfatter en aldrende befolkning, øget forekomst og udbredelse af kræft, hjertesvigt, fedme, type 2-diabetes og fysisk inaktivitet. Den øgede brug af computertomografi (CT) og forbedringer i CT-teknikkerne har øget muligheden for at opdage lungeemboli.
- I øjeblikket er livstidsrisikoen for at udvikle venøs tromboemboli 8 % for personer i alderen 45 år (Raskob et al, Heit et al).
Kardiopulmonale effekter af lungeemboli
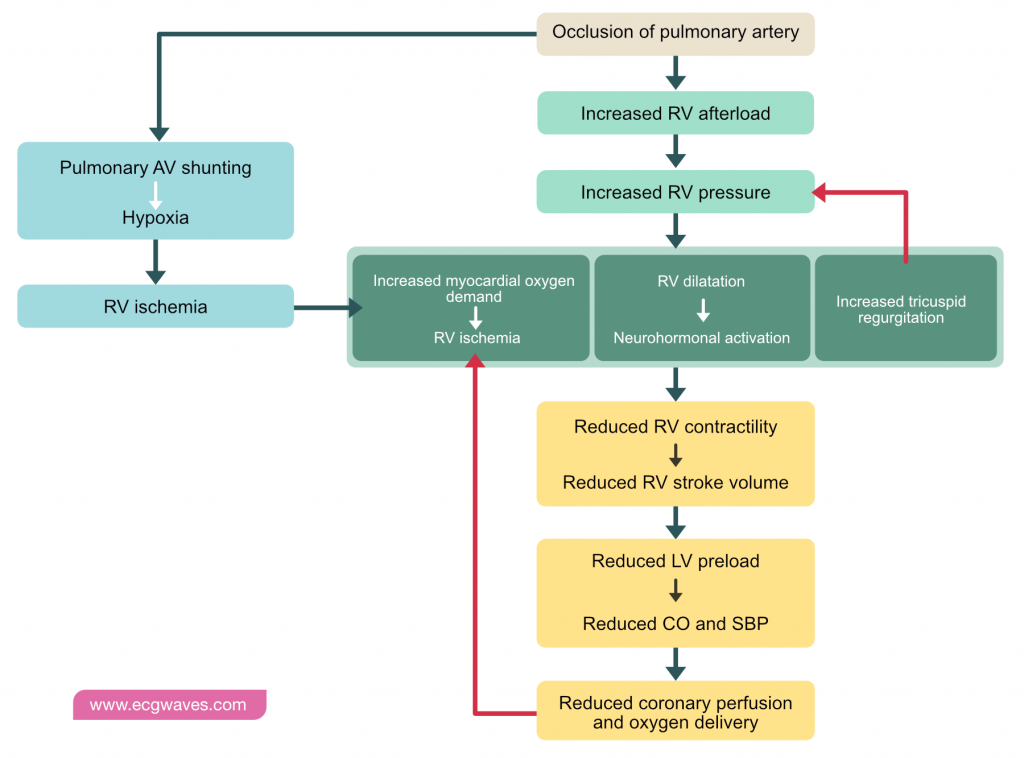
Hæmodynamiske effekter
Lungeemboli fører til øget modstand i hovedlungearterien og dermed øget afterload på højre ventrikel. Dette øger belastningen på højre ventrikel, som derfor kræver mere ilt. Stigningen i afterload resulterer også i et øget intramuralt tryk i højre ventrikel, hvilket modvirkes af en dilatation af ventriklen. Dilatation af højre ventrikel resulterer i reduceret intraventrikulært tryk og dermed reduceret myoardial belastning.
Lungeemboli forårsager øget belastning af højre ventrikel, hvilket resulterer i øget iltbehov og dilatation af højre ventrikel.
På trods af dilatationen vil der udvikles myokardieiskæmi, hvis iltbehovet i højre ventrikel overstiger ilttilførslen. Langvarig og udtalt iskæmi fører til højre ventrikelinfarkt. Uanset om der udvikles et infarkt eller ej, resulterer dilatationen, den øgede efterbelastning og iskæmien i et reduceret slagvolumen i højre ventrikel. Når højre ventrikels slaggevolumen mindskes, pumpes der mindre blod ind i venstre ventrikel, hvilket fører til nedsat forspænding af venstre ventrikel. Faldende forbelastning fører til et fald i hjertets output og et efterfølgende fald i det systoliske blodtryk. Reduceret minutvolumen og reduceret blodtryk giver en reduktion i koronar perfusionstryk, herunder perfusion gennem den højre koronararterie (RCA). Dette forværrer iskæmien i højre ventrikel yderligere. Højre ventrikels slagvolumen falder mere, hvilket fører til yderligere reduktioner i venstre ventrikels preload, og cyklussen gentager sig.
Det gradvise fald i hjertets minutvolumen, systolisk blodtryk og koronar perfusion vil i sidste ende resultere i hjertestop, typisk med pulsløs elektrisk aktivitet (PEA) på EKG.
Akut belastning af højre ventrikel kaldes også højre ventrikelstamme.
Pulmonale effekter
Obstruktion af lungearterier fører til hypoxi i lungeparenkym og pleura. Langvarig hypoxi resulterer i parenkymbetændelse og i sidste ende infarkt (dvs. lungeinfarkt). Dette manifesterer sig med brystsmerter; typisk pleuritiske brystsmerter (skarp smerte korreleret med vejrtrækning). Lungeinfarkt fører til parenkymatisk blødning, som viser sig ved hæmoptyse.
Okklusionen fører også til et misforhold mellem ventilation og perfusion (dvs. der er ventilerede områder, som ikke perfunderes), hvilket resulterer i reduceret iltning af blodet. Dette resulterer i nedsat arterielt ilttryk (PaO2) og iltmætning (hypoxi). Refleksiv hyperventilation kan føre til respiratorisk alkalose med hypokapni (reduceret PaCO2).
Symptomer og tegn på lungeemboli
De fleste tilfælde af lungeemboli har akut indsættende symptomer. Udbruddet kan være relateret til ændringer i kropsstilling eller fysisk aktivitet. Det kan antages, at aktiviteten eller ændringen i kropsstilling forårsager løsrivelse af venøse tromber, som derefter bevæger sig til hjertet.
Symptomerne afhænger af de hæmodynamiske effekter af okklusionen, som bestemmes af emboliens størrelse og placering, hjertefunktion og komorbiditet. Små lungeembolier kan være asymptomatiske, mens store proksimale okklusioner hurtigt kan forårsage kredsløbskollaps og hjertestop.
De mest almindelige symptomer og tegn ved lungeemboli er som følger:
- 50 % har dyspnø og takypnø.
- 50 % har brystsmerter, typisk pleuritiske brystsmerter.
- Takykardi er det mest almindelige EKG-fund (se EKG ved lungeemboli nedenfor).
- Udspilet halsvene (på grund af forhøjet tryk i højre ventrikel).
- Hoste.
- Hæmoptyse.
- Hypotension.
- Væsentligt fald i systolisk blodtryk.
- Synkope, præ-synkope.
- Feber.
- Tegn på dyb venetrombose (DVT) eller anden venøs trombose.
Hypotension, fald i systolisk blodtryk, præ-synkope eller synkope er stærke prædiktorer for massiv lungeemboli.
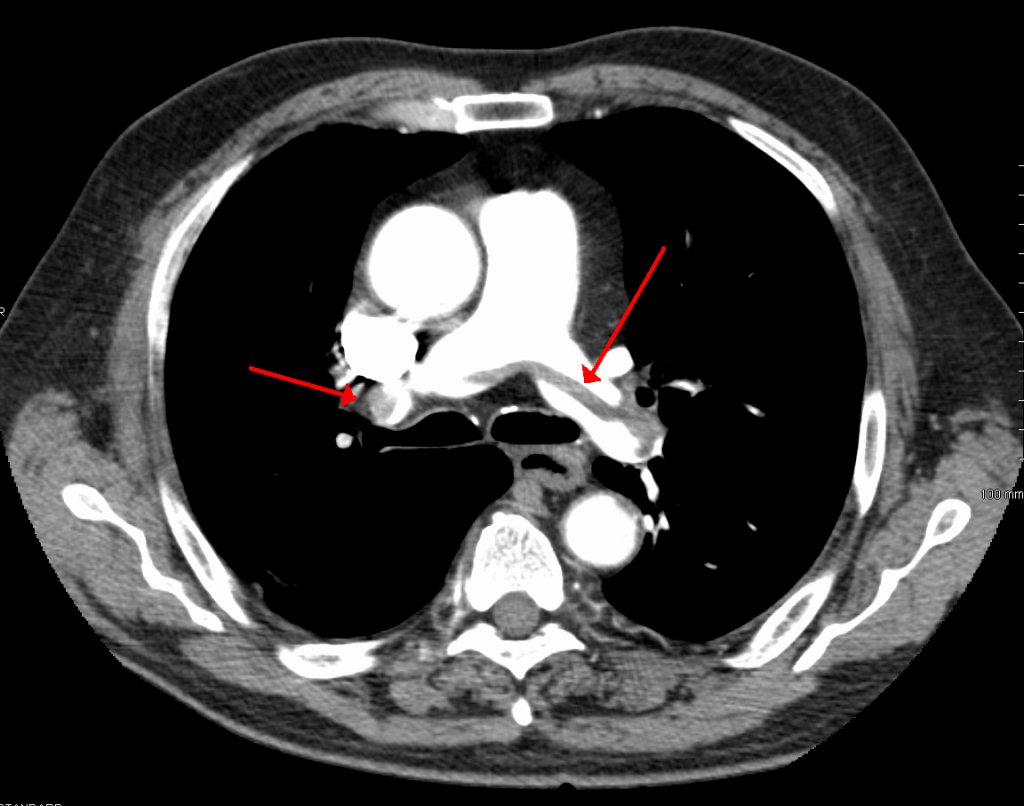
Sadel-lungeemboli
Sadel-lungeemboli refererer til en stor embolus, der skræver over bifurkationen af lungestammen, hvor dele af embolus strækker sig ind i venstre og højre lungearterie. Emboliens kontur på CT-scanninger kan ligne en hestesaddel (figur 1). Sadelembolier forårsager alvorlige hæmodynamiske effekter.
Årsager til lungeemboli
De mest almindelige årsager til lungeemboli er som følger:
- Dyb venetrombose (DVT) er den mest almindelige årsag.
- Fedtemboli opstår efter operationer, herunder ortopædiske indgreb.
- Cementemboli refererer til embolisering af polymethylmethacrylat (PMMA) i lungearterierne. PMMA bruges primært til perkutan vertebroplastik.
- Luftemboli.
- Fostervandsemboli.
- Vævsemboli.
- Tumoremboli.
- Bakteriel emboli.
Risikofaktorer for lungeemboli
Risikofaktorer for lungeemboli er som følger (Di Nisio et al):
Hyperkoagulabilitet
- Stigende alder
- Kræft
- Antifosfolipid-syndrom
- Østrogenbehandling
- Graviditet
- Perioden efter fødslen (8 uger)
- Arvelighed for venøs tromboembolisme
- Fedme
- Dehydrering
- Inflammatorisk tarmsygdom (Crohns sygdom, colitis ulcerosa)
Indgreb og traumer
- Kirurgi
- Traumer
- Frakturer
- Implantation af udstyr (f.eks. centralt venekateter, pacemaker, ICD, CRT).
Immobilisering og hospitalsindlæggelse
- Indlæggelse på hospital
- Lange rejser (>3 timer siddende)
- Lammelse, parese
Arvelige lidelser
- Faktor V Leiden-mutation
- Prothrombin-mutation
- Antitrombin-mutation
- Protein C-mangel
- Protein S-mangel
Genetisk hyperkoagulabilitet bør mistænkes, hvis patienten er ung, mangler risikofaktorer for tromboembolisme, har arvelighed eller oplever tilbagevendende embolier.
Bemærk, at 30-50% af alle venøse tromboembolier er uprovokerede. De resterende er fremkaldt af en eller flere af de faktorer, der er nævnt ovenfor.
Diagnose af lungeemboli
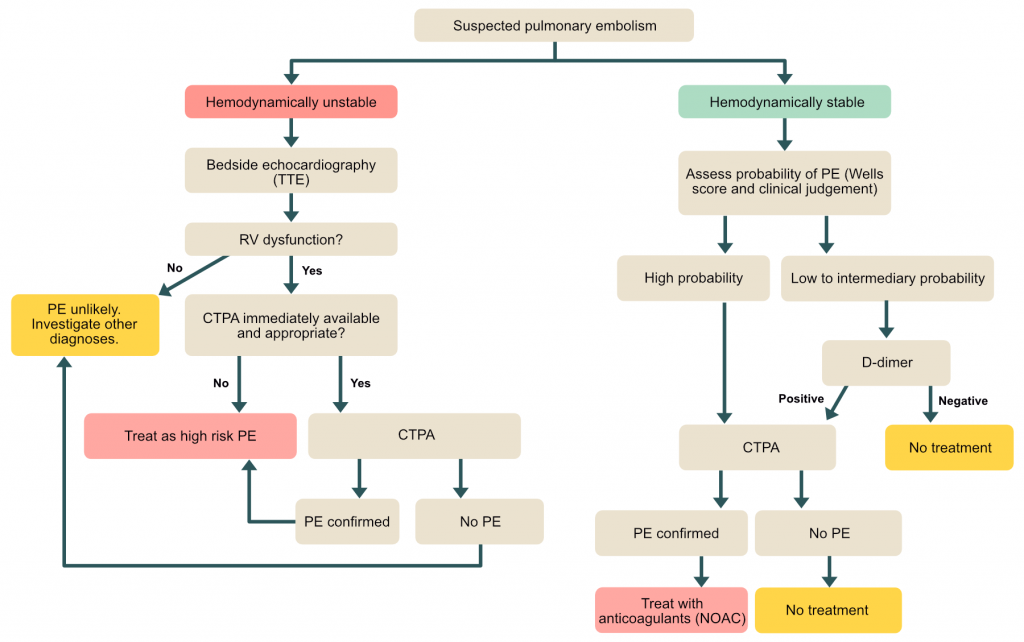
Pre-test-sandsynlighed for lungeemboli
Pre-test-sandsynlighed er et statistisk udtryk, der bruges til at vejlede om behandlinger og undersøgelser. Hvis prætestsandsynligheden for lungeemboli er meget høj, er det meget sandsynligt, at patienten har lungeemboli, hvilket gør det unødvendigt at analysere D-dimer. På samme måde, hvis der ikke er sandsynlighed for lungeemboli, er CT-scanning måske ikke berettiget, medmindre D-dimer er positiv (forhøjet). Pre-test-sandsynligheden vurderes hos alle patienter med mistanke om lungeemboli.
Pre-test-sandsynligheden for lungeemboli vurderes med en af følgende forudsigelsesmodeller (scores):
- Wells-score
- Modificeret Wells-score
- Revideret Genève-score
- PERC (kriterier for udelukkelse af lungeemboli)
Wells-score og modificeret Wells-score kan bruges under indlæggelse og i ambulant regi. PERC bruges til at udelukke lungeemboli.
Hvis den kliniske mistanke om lungeemboli er høj, bør patienten gennemgå en computertomografisk scanning, uanset score og D-dimer.
Wells-score for lungeemboli
Wells-score for lungeemboli må ikke forveksles med Wells-score for DVT. Nedenstående risikomodel (score) anvendes kun i tilfælde af mistanke om lungeemboli.
Tabel 1. Wells-kriterier for lungeemboli
| KRITERIER | PUNKTER |
|---|---|
| Symptomer eller tegn på DVT | 3 |
| Lungeemboli mere sandsynlig end andre diagnoser | 3 |
| Tidligere VTE (lungeemboli eller DVT) | 1.5 |
| Takykardi (HR >100/bpm) | 1.5 |
| Immobilisering eller operation inden for de sidste 4 uger | 1.5 |
| Hæmoptyse | 1 |
| Kræft | 1 |
Evaluering af Wells-score
Wells-score, original
- 0-1 point: Lav sandsynlighed (6 % absolut risiko).
- 2 til 6 point: Mellemstor sandsynlighed (23 % absolut risiko)
- ≥7 point: Høj sandsynlighed (50 % absolut risiko)
Wells-score, modificeret
- ≤ 4 point: Lungeemboli ikke sandsynlig (8 % absolut risiko)
- ≥ 5 point: Lungeemboli sandsynlig (34% absolut risiko).
Revideret Genève-score for lungeemboli
Tabel 2. Revideret Genève-score for lungeemboli
| KRITERIER | PUNKTER |
|---|---|
| Alder >65 år | 1 |
| Tidligere VTE (PE eller DVT) | 3 |
| Nylig operation (hvilken som helst) eller underekstremitetsfraktur | 2 |
| Kræftsygdom | 2 |
| Ensidige smerter i benet | 3 |
| Hæmoptyse | 2 |
| Hjertefrekvens 75-94 bpm | 3 |
| Hjertefrekvens ≥ 95/min | 5 |
| Smerter ved palpation af underekstremitet med ensidigt ødem | 4 |
Evaluering af Genève-score
- <4 point: lav sandsynlighed for lungeemboli (9 % absolut risiko)
- 4 til 10 point: mellemstor sandsynlighed for lungeemboli (26 % absolut risiko)
- >10 point: høj sandsynlighed for lungeemboli (76% absolut risiko)
Kriterier for udelukkelse af lungeemboli (PERC)
Hvis sandsynligheden for lungeemboli er lav (i henhold til Wells-score eller Geneva-score), kan PERC bruges til at udelukke lungeemboli.
Tabel 3. Kriterier for udelukkelse af lungeemboli (PERC)
| KRITERIER | PUNKTER |
|---|---|
| Alder > 50 år | 1 |
| Hjertefrekvens > 100/min | 1 |
| Iltmætning (POX) < 95 % | 1 |
| Hæmoptyse | 1 |
| Østrogenbehandling | 1 |
| Tidligere VTE (lungeemboli eller blodprop i hjertet) | 1 |
| Nylig (<4 uger) operation (hvilken som helst) eller traume | 1 |
| Ensidigt ødem i underekstremiteterne | 1 |
Evaluering af PERC-score
- 0 point: lav sandsynlighed (< 1 %). Lungeemboli meget usandsynlig.
- ≥1 point: Lungeemboli kan ikke udelukkes, og yderligere undersøgelser er påkrævet.
D-dimer
D-dimer er et biprodukt, der produceres under nedbrydning af fibrinogen. Derfor indikerer forhøjede D-dimer-niveauer nylig fibrinolyse.
D-dimer analyseres, hvis sandsynligheden for lungeemboli er lav til middel. D-dimer har meget høj sensitivitet for venøs tromboemboli, herunder lungeemboli; stort set alle patienter med lungeemboli udviser forhøjede D-dimer-niveauer. Specificiteten er dog lav, hvilket skyldes, at D-dimer-niveauerne stiger i alle situationer med trombose.
Negativ D-dimer udelukker lungeemboli (og DVT), hvis den kliniske mistanke er lav til middel. Hvis den kliniske mistanke om lungeemboli er høj, må D-dimer ikke bruges til at udelukke lungeemboli.
Andre biomarkører
- Elektrolytter, nyrefunktion (estimeret GFR) og leverfunktion skal vurderes hos alle patienter.
- Troponin (troponin T, troponin I) analyseres for at afgøre, om der er sket et myokardieinfarkt. Forhøjede troponinniveauer indikerer højre ventrikelinfarkt, som er prognostisk ugunstigt.
- Det er ikke nødvendigt at analysere blodgas (arteriegas). Resultaterne viser typisk respiratorisk alkalose, reduceret ilttryk (PaO2) og forhøjet pH.
EKG ved lungeemboli
EKG ‘et kan bruges til at finde yderligere tegn på lungeemboli. Sensitivitet og specificitet er lav for alle EKG-kriterier, der er foreslået til påvisning af lungeemboli.
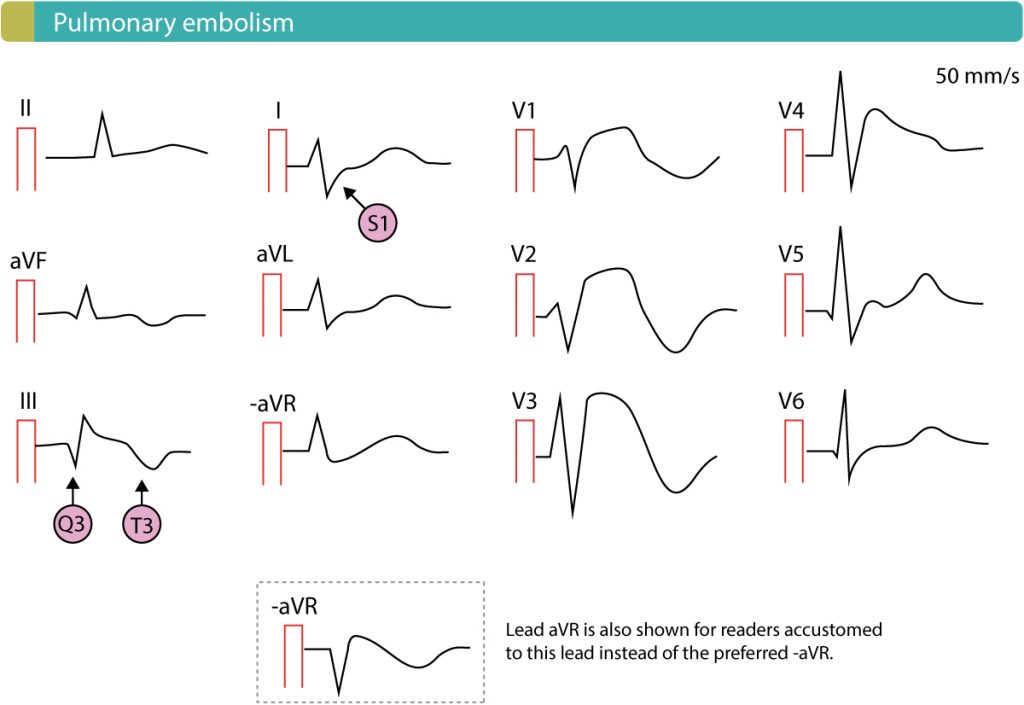
Følgende EKG-ændringer kan ses ved lungeemboli:
- S1Q3T3-mønster henviser til tilstedeværelsen af en dyb S-bølge i afledning I og en dyb Q-bølge i afledning III samt T-bølgeinversion i afledning III.
- T-bølge-inversioner (negative T-bølger) i V1-V4.
- Nyopstået komplet eller inkomplet højre grenblok (RBBB).
- Nyopstået atrieflimren, atrieflagren eller atrialtakykardi.
- ST-elevation eller ST-depression i V1-V3.
- P pulmonale
- Afvigelse af højre akse (RAD).
Sinustakykardi er det mest almindelige EKG-fund ved lungeemboli.
Computertomografi af lungearterierne (CTPA)
Computertomografi af lungearterierne (CTPA) er den foretrukne billeddannelsesmetode ved mistanke om lungeemboli. Undersøgelsen, som er kontrastforstærket, er hurtig, har høj sensitivitet og høj specificitet.
Akut lungeemboli diagnosticeres, når CTPA viser komplette eller delvise fyldningsdefekter i lungearterierne. Delvise fyldningsdefekter kan være centralt eller perifert placeret i arterien og vil være omgivet af kontrast (Leitman et al.).
Indirekte tegn på lungeemboli omfatter pleuravæske eller kileformet lungeinfarkt.
Computertomografi bør undgås i følgende situationer:
- Graviditet.
- Allergi over for kontrast.
- Nyresvigt.
Lungescintigrafi
Lungescintigrafi udføres, hvis CTPA er uhensigtsmæssig på grund af graviditet, kontrastmiddelallergi eller nyresvigt. Scintigrafi er tidskrævende og kræver lave doser af radioaktive markører. Pulmonal perfusion sammenlignes med pulmonal ventilation, og enhver regional uoverensstemmelse, kaldet mismatch, i ventilation og perfusion tyder på lungeemboli.
Ekkokardiografi
Ekkokardiografi anbefales for at visualisere indirekte tegn på lungeemboli og belastning af højre ventrikel. Følgende ekkokardiografiske fund tyder på akut lungeemboli:
- Øget tricuspid regurgitation (TI).
- Forhøjet PASP (systolisk PA-tryk).
- Dilateret vena cava inferior med tab af respiratorisk variation.
- Dilatation af højre ventrikel.
- Paradoksal septumbevægelse.
Andre billeddannelsesmetoder
Pulmonal angiografi udføres i udvalgte tilfælde, især hvis endovaskulær behandling er mulig.
Magnetisk resonans har høj sensitivitet og specificitet og kan udføres, hvis diagnosen er uklar, eller hvis andre modaliteter ikke er mulige.
Behandling af lungeemboli
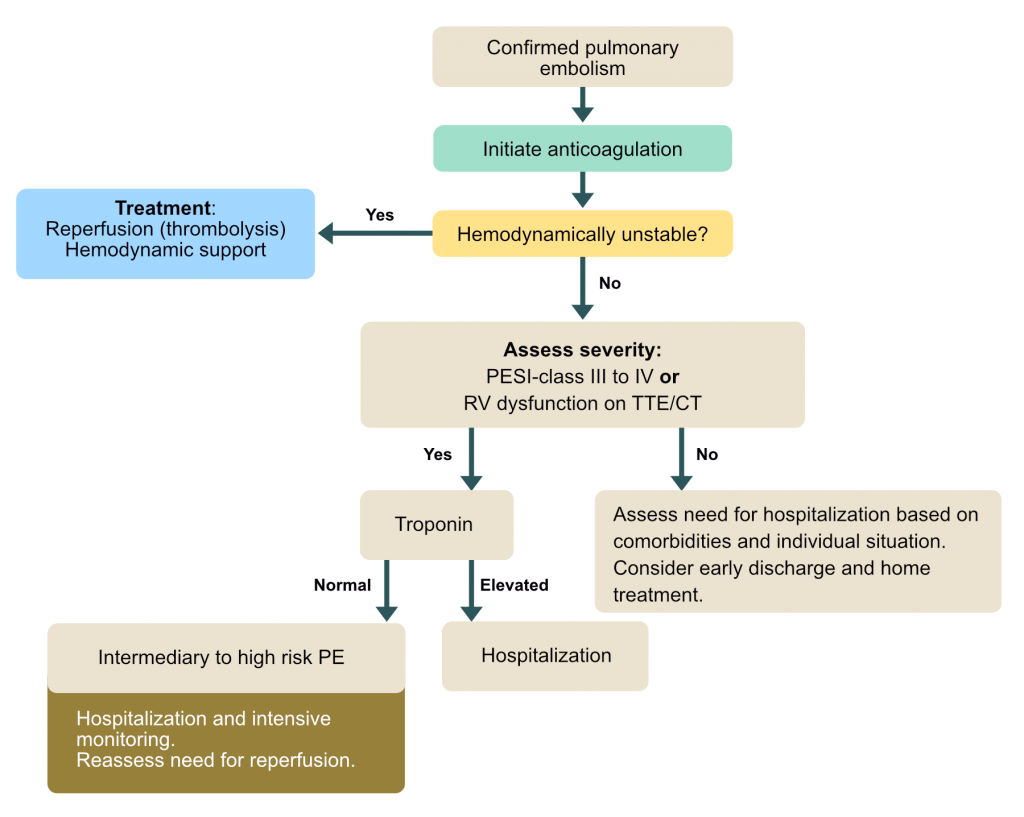
I den akutte situation styres behandlingen af patientens hæmodynamiske tilstand. Alvorlig lungeemboli (massiv lungeemboli) behandles med øjeblikkelig antikoagulation og reperfusion (trombolyse). Lungeemboli uden hæmodynamiske effekter behandles med antikoagulantia.
Alvorlig (massiv lungeemboli) defineres som lungeemboli, der opfylder et af følgende kriterier:
- Systolisk blodtryk <90 mm Hg
- >40 mm Hg fald i systolisk blodtryk.
Der er dog yderligere advarselstegn:
- Synkope, præ-synkope, svimmelhed.
- Takykardi.
- Højre ventrikeldilatation, forhøjet PASP.
- Paradoksal septumbevægelse.
- Forhøjet BNP eller NT-proBNP eller troponin.
Risikostratificering af lungeemboli: PESI (Pulmonal Embolism Severity Index)
PESI estimerer 30-dages dødelighed blandt patienter med bekræftet lungeemboli. PESI bruges til at guide den indledende behandling.
Tabel 4. PESI (Pulmonal Embolism Severity Index)
| KRITERIER | POINTER |
|---|---|
| Alder | 1 pr. år |
| Kræft | 30 |
| Systolisk blodtryk < 100 mm Hg | 30 |
| Hjertefrekvens ≥ 110/min | 20 |
| Iltmætning (POX) < 90% | 20 |
| Hjertesvigt | 10 |
| Lungesygdom | 10 |
| Ændret mental status | 60 |
| Kropstemperatur <96,8°F eller <37°C | 20 |
| Åndedrætsfrekvens ≥ 30/min | 20 |
| Mandligt køn | 10 |
Evaluering af PESI-score
| PESI-KLASSE | PESI-PUNKTER | RISIKO | 30-DAGES DØDELIGHED | DØDELIGHED PÅ HOSPITALET |
|---|---|---|---|---|
| Klasse I | <66 | Meget lav risiko | 0-1.6% | ≤1.1% |
| Klasse II | 66-85 | Lav risiko | 1.7-3.5% | ≤1.9% |
| Klasse III | 86-105 | Mellemliggende risiko | 3.2-7.1% | ≤4.7% |
| Klasse IV | 106-125 | Høj risiko | 4.0-11.4% | ≤7.0% |
| Klasse V | > 125 | Meget høj risiko | 10.0-23.9% | ≤17.2% |
Behandling af højrisiko (massiv) lungeemboli
Højrisiko-lungeemboli (30-dages mortalitet >15%) er synonymt med massiv lungeemboli. Disse patienter har systolisk blodtryk <90 mm Hg, alternativt >40 mm Hg fald i systolisk blodtryk. Langt de fleste af disse patienter har brug for trombolyse. Hurtig ekkokardiografi (TTE) og CT-scanning er vigtig.
Umiddelbare handlinger
- Start infusion med heparin med lav molekylvægt (f.eks. enoxaparin).
- Giv ilt, hvis iltmætningen er <95 %.
- Overvej at give en væskebolus (500 ml).
- Giv inotropisk støtte (f.eks. noradrenalin), hvis patienten er hypotensiv.
- Find ud af, om der er kontraindikationer for trombolyse. Hvis der ikke er kontraindikationer, gives alteplas:
- Alteplas i.v. 10 mg i 2 minutter og 90 mg infusion i 120 minutter.
- Maks. dosis er 1,5 mg/kg for patienter, der vejer <65 kg.
- Heparininfusionen sættes på pause under trombolysen og genoptages tidligst 60 minutter efter afslutning af alteplasinfusionen.
Kateterbaseret lokal trombolyse eller trombektomi kan være at foretrække i særlige situationer, eller hvis trombolyse ikke giver reperfusion. Kirurgisk trombektomi kan også overvejes, afhængigt af lokale rutiner.
Kontraindikationer for trombolyse
Absolutte kontraindikationer
- Strukturel intrakraniel sygdom
- Tidligere hjerneblødning
- Tidligere iskæmisk slagtilfælde <3 måneder
- Igangværende blødning
- Nylig rygmarvs- eller hjertekirurgi
- Hovedtraume eller hjerneskade
- Hypokoagulabilitet
Relative kontraindikationer for trombolyse
- Systolisk blodtryk >180 mm Hg eller diastolisk >110 mm Hg
- Nylig blødning (ikke intrakraniel)
- Nylig operation (andet end hjerte- eller rygmarvskirurgi)
- Nylig invasiv procedure
- Iskæmisk slagtilfælde i >3 måneder siden
- Brug af antikoagulantia
- Perikardieeffusion
- Diabetisk retinopati
- Graviditet
- Alder >75 år
- Kropsvægt <60 kg
Behandling af lungeemboli med lav til intermediær risiko
Lungeemboli med lav til intermediær risiko behandles med nye orale antikoagulantia (NOAK). NOAK giver 30 % lavere risiko for alvorlige blødninger sammenlignet med warfarin. Følgende principper gælder for behandling af patienter med lungeemboli:
Indledende behandling
- Hvis dabigatran eller edoxaban vælges til langtidsbehandling, er 5 dages indledende behandling med lavmolekylært heparin (LMWH) påkrævet.
- Hvis rivaroxaban eller apixaban vælges til langtidsbehandling, er det ikke nødvendigt med forbehandling med LMWH.
- Egnede LMWH omfatter enoxaparin til patienter med normal nyrefunktion. Patienter med nyresvigt behandles med ufraktioneret heparin (UFH). UFH foretrækkes også til patienter, som senere kan få brug for trombolyse.
- LMWH foretrækkes som indledende og langvarig behandling hos gravide kvinder og personer med kræft.
Langtidsbehandling
- LMWH foretrækkes til gravide kvinder og personer med kræft.
- For warfarin er den terapeutiske PK-INR 2 til 3.
- NOAC-doser:
- Dabigatran: 150 mg x 2
- Edoxaban: 60 mg x 1
- Rivaroxaban: 15 mg x 2 i 21 dage, derefter 20 mg x 2
- Apixaban: 10 mg x 2 i 7 dage, derefter 5 mg x 2.
Evaluering af blødningsrisiko
Der er ikke udviklet nogen specifik risikomodel for lungeemboli. HAS-BLED bruges ofte, på trods af at den blev valideret til at vurdere blødningsrisikoen hos patienter med atrieflimren. Risikofaktorer for blødning omfatter følgende:
- Høj alder
- Skrøbelighed
- Tidligere blødningshændelser
- Kræft
- Nyresvigt
- Leversvigt
- Trombocytopeni
- Slagtilfælde
- Sukkersyge
- Anæmi
- Behandling med blodpladehæmmere eller antikoagulantia.
- Nylig operation
Langsigtede komplikationer af lungeemboli
- Pulmonal hypertension udvikler sig hos <5%.
- Hjertestop.
- Højre ventrikel svigt (se Hjertesvigt).
- Lungeinfarkt (10 % af tilfældene).
- Pleural effusion
- Post-trombotisk syndrom (30 %).
Referencer
Di Nisio et al. Dyb venetrombose og lungeemboli. Lancet 2016;388:3060-73
Raskob GE, Angchaisuksiri P, Blanco AN, et al. Thrombosis:
a major contributor to global disease burden. Arterioscler Thromb Vasc Biol 2014; 34: 2363-71
Heit JA. Epidemiologi af venøs tromboembolisme. Nat Rev Cardiol 2015; 12: 464-74.
Kearon C et al. Natural history of venous thromboembolism. Cirkulation 2003; 107: I22-30.
Goldhaber SZ, Visani L, De Rosa M. Akut lungeemboli: kliniske resultater i International Cooperative Pulmonary Embolism Registry (ICOPER). Lancet 1999; 353: 1386-89.
Konstantinides et al. 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society. European Heart Journal (2020) 41, 543603.
Leitman et al. Pulmonal arteries: imaging of pulmonary embolism and beyond. Cardiovasc Diagn Ther. 2019 Aug; 9 (Suppl 1): S37-S58
